Ишемические поражения толстой кишки у пациентов с метаболическим синдромом
- Аннотация
- Статья
- Ссылки
- English
Однако у пациентов с МС изменения со стороны толстой кишки выявляются в 58,5% случаев и имеют клинико-морфологические признаки микроишемического колита (МИК). Микроскопический ишемический колит представляет собой одну из форм циркуляторно-гипоксического поражения кишечника и характеризуется структурными изменениями слизистой оболочки и других слоев толстой кишки.
Патогенез МИК обусловлен рядом факторов, среди которых важное значение отводится нарушению микроциркуляции слизистой оболочки толстой кишки, дисбиотическим нарушениям и нарушениям моторики толстой кишки. При МС, основными дефинициями которого являются абдоминальное ожирение и инсулинорезистентность, создаются предпосылки для реализации указанных патогенетических механизмов.
В статье рассмотрены особенности течения МИК, критерии его диагно-стики и подходы к лечению.
Однако у пациентов с МС изменения со стороны толстой кишки выявляются в 58,5% случаев и имеют клинико-морфологические признаки микроишемического колита (МИК). Микроскопический ишемический колит представляет собой одну из форм циркуляторно-гипоксического поражения кишечника и характеризуется структурными изменениями слизистой оболочки и других слоев толстой кишки.
Патогенез МИК обусловлен рядом факторов, среди которых важное значение отводится нарушению микроциркуляции слизистой оболочки толстой кишки, дисбиотическим нарушениям и нарушениям моторики толстой кишки. При МС, основными дефинициями которого являются абдоминальное ожирение и инсулинорезистентность, создаются предпосылки для реализации указанных патогенетических механизмов.
В статье рассмотрены особенности течения МИК, критерии его диагно-стики и подходы к лечению.
Введение
Одним из важных патогенетических механизмов абдоминального ожирения и сахарного диабета (СД) 2 типа – основных компонентов метаболического синдрома (МС) – является дисбиоз толстой кишки. Эндотоксин-опосредованное усиление процессов перекисного окисления липидов и накопления свободных радикалов играет ключевую роль в развитии атерогенной дислипидемии и системного, хронического, субклинически протекающего воспаления. Атерогенная дислипидемия и воспаление в свою очередь обусловливают развитие атеросклероза.
Установлено, что кишечная микрофлора участвует в конечных этапах метаболизма холестерина, желчных кислот, углеводов и белков. Кишечные бактерии метаболизируют поступивший в толстую кишку холестерин в копростанол и способны осуществлять глубокий гидролиз молекулы холестерина. В результате анаэробной деятельности микроорганизмов толстой кишки образуются летучие кислоты – уксусная, пропионовая, п-масляная, изомасляная, изовалериановая. Данные кислоты признаны важнейшими регуляторами водного, электролитного и кислотно-щелочного баланса.
Поскольку макроорганизм и его микрофлора представляют единую экологическую систему, многие метаболические заболевания ассоциируются с нарушением микробного сообщества тонкой кишки. Изменение кишечной микрофлоры вызывает повышенное поступление в кровь эндотоксина, который, как было отмечено выше, считается важным звеном формирования МС, атеросклероза, СД 2 типа, ожирения.
Дисбиотические нарушения в толстой кишке при МС усиливают хронические циркуляторные расстройства. С последними ассоциируется ишемическое поражение толстой кишки (ИПТК). Хроническое нарушение кровотока в бассейне брюшного отдела аорты и ее непарных висцеральных ветвей приводит к ишемии органов брюшной полости.
Степень ИПТК зависит от состояния кровотока в брыжеечных артериях. Верхняя брыжеечная артерия (ВБА) обеспечивает кровоснабжение проксимальных отделов толстой кишки до селезеночного изгиба, нижняя – ее дистальных отделов. Характерной особенностью системы кровоснабжения ободочной кишки является наличие коллатералей с верхней брыжеечной артерией и дугой Риолана – параллельным или краевым сосудом, идущим вдоль брыжеечного края. При сужении нижней брыжеечной артерии происходят сегментарные ишемические поражения селезеночного изгиба, илеоцекального и ректосигмоидального отделов.
Кровоснабжение свободного края ободочной кишки значительно хуже, чем брыжеечного, поэтому слизистая оболочка толстой кишки поражается неравномерно.
В отличие от толстой кишки прямая кишка редко вовлекается в патологический процесс при хронической абдоминальной ишемии. Ее кровоснабжение осуществляется по верхней и нижней прямокишечным артериям, между которыми имеется богатая сеть интрамуральных анастомозов.
В настоящее время ИПТК рассматривается как микроскопический ишемический колит (МИК).
Ишемический колит представляет собой одну из форм циркуляторно-гипоксического поражения кишечника. Для него характерны структурные изменения слизистой оболочки и других слоев толстой кишки [1]. Ишемический колит чаще встречается у лиц пожилого возраста, страдающих ишемической болезнью сердца (ИБС), артериальной гипертензией (АГ) и распространенным атеросклерозом, СД 2 типа [1, 2–4]. Дополнительным фактором его развития является нарушение тканевого метаболизма.
Согласно последним данным нарушение микроциркуляции может быть обусловлено дислипопротеинемией, нарушениями свертывающей системы крови, инсулинорезистентностью, гипотиреозом, висцеральной полинейропатией.
Клинические проявления и диагностика
На данный момент оценить истинную распространенность МИК сложно, что обусловлено вариабельностью и неспецифичностью симптомов. Согласно результатам исследований, проведенных в Московском клиническом научно-практическом центре им. А.С. Логинова, МИК встречается у 58% пациентов с МС, у 78–80% больных старших возрастных групп.
Как показывает практика, для диагностики МИК следует провести анамнестические, клинические, лабораторно-инструментальные и морфологические исследования толстой кишки и оценку показателей висцерального кровотока.
В клиническом отделении Центрального научно-исследовательского института гастроэнтерологии обследовали 52 пациентов с МС и сопутствующими сердечно-сосудистыми заболеваниями. Среди них 24 мужчины и 28 женщин. Возраст больных варьировался от 56 до 80 лет, в среднем – 63,5 ± 2,7 года.
При сборе анамнеза особое внимание обращали на наличие сердечно-сосудистых заболеваний (ИБС, АГ, цереброваскулярной болезни, атеросклероза сосудов нижних конечностей), сосудистых катастроф (инфаркта миокарда, острого нарушения мозгового кровообращения), оперативных вмешательств на сосудах (аортокоронарного шунтирования, протезирования брюшного отдела аорты), ожирения, СД 2 типа и других компонентов МС, патологий щитовидной железы, неалкогольной жировой болезни печени и других метаболических заболеваний. Особо значимыми были внеабдоминальные и абдоминальные боли, тяжесть сопутствующих сердечно-сосудистых заболеваний, выраженность факторов сердечно-сосудистого риска.
При осмотре оценивали пальпаторные и аускультативные признаки поражения брюшной аорты и других сосудов (наличие пульсации, систолического шума в проекции аорты).
Определяли липидный спектр крови (общий холестерин, холестерин липопротеинов низкой и высокой плотности, триглицериды) и показатели вязкости крови.
Проводили ультразвуковое исследование сосудов: диаметр брюшной аорты, толщина ее стенки, наличие кальцинатов и пристеночных тромбов, а также допплеровское исследование аорты и ее непарных висцеральных артерий. В первом случае использовали аппарат «RТ-Х-200», во втором – «Алока-1100».
Изучали гемодинамику артериального русла, в частности максимальную и минимальную линейную скорость кровотока, среднюю скорость кровотока, индекс пульсации, индекс резистентности, систоло-диастолическое соотношение, качественную характеристику спектра частот допплеровских кривых.
Проводили колоноскопию или ирригоскопию для выявления особенностей моторной функции и воспалительных изменений в толстой кишке, таких как отек, геморрагии, эрозивно-язвенные поражения, псевдодивертикулы, псевдополипы и стриктуры, часто обнаруживаемые у больных ИПТК [5–8].
Выполняли гистологическое исследование cлизистой оболочки толстой кишки.
У 40 пациентов диагностирована АГ, у 42 – ИБС, у 39 – цереброваскулярная болезнь, у 17 – атеросклероз сосудов нижних конечностей. Инфаркт миокарда ранее перенесли восемь больных, инсульт – пять, аортокоронарное шунтирование – один, протезирование брюшной аорты – двое больных. У трех пациентов выявлена аневризма брюшной аорты.
Сахарным диабетом страдали 39 обследованных. Нарушение толерантности к глюкозе выявлено у 13 пациентов, ожирение – у 48.
Патология щитовидной железы (узловой зоб, аутоиммунный тиреоидит – чаще в стадии эутиреоза на фоне заместительной терапии) имела место у семи больных. Двое из них перенесли субтотальную резекцию щитовидной железы.
Абдоминальный болевой синдром разной степени тяжести наблюдался у всех пациентов. У 29 (69%) из них боль локализовалась в верхней части живота, у 11 (26%) – в левой части живота, у 15 (36%) – в нижней части живота. Отмечались также мигрирующие боли.
У 44 (81%) пациентов боли были ноющими, периодическими или постоянными, у 2 (4,8%) – пульсирующими, у 4 (9,5%) – схваткообразными.
Тяжесть и дискомфорт в эпигастральной и мезогастральной областях после еды ощущали 13 (31%) больных. Половина больных отмечала связь между абдоминальной болью и приемом пищи или физической нагрузкой.
По мере прогрессирования заболевания происходило истощение организма из-за ситофобии (страха возникновения боли после приема пищи), что считается характерным признаком абдоминального ишемического синдрома [4, 5, 7].
Метеоризм и урчание в животе отмечали 34 и 21% больных соответственно. На запоры жаловались 38% пациентов, диарею – 24%, неустойчивый стул – 24% пациентов.
У 35 (60%) больных выслушивался систолический шум над брюшным отделом аорты, у 39 (70%) – она была уплотненной, болезненной и расширенной. При пальпации отмечались вздутие живота, шум в виде плеска в слепой кишке, болезненность и спастическое сокращение сигмовидной кишки.
Полученные при обследовании данные позволили предположить наличие МИК.
Согласно результатам лабораторного исследования крови у 11 пациентов был умеренно повышен уровень гемоглобина и эритроцитов, что является косвенным признаком нарушения микроциркуляции и гемореологии. Подтверждением тому стали результаты коагулограммы, проведенной у 27 больных. У 17 из них выявлены признаки гиперкоагуляции, у 10 – гипокоагуляции.
Нарушение липидного спектра крови зафиксировано у 72% больных. У 24% из них наблюдалась дислипопротеинемия IIА типа, у 9% больных – гипертриглицеридемия.
При проведении ультразвукового исследования у 39 больных обнаружены признаки атеросклеротического поражения брюшного отдела аорты: неровность и утолщение стенок, пристеночные кальцинаты. У двух пациентов выявлена аневризма брюшного отдела аорты с расширением инфраренального отдела до 3,8 см и пристеночным флотирующим тромбом.
Допплеровское исследование проведено 40 пациентам. У всех обнаружено поражение от двух до четырех сосудов. У 30 из них наблюдались качественные и количественные признаки нарушения кровотока по чревному стволу (ЧС), общей печеночной артерии (ОПА), селезеночной артерии (СА), у 13 – по ВБА. Качественные признаки нарушения кровотока по ЧС, ОПА, СА обнаружены у 34 пациентов, у 13 из них – по ВБА. Количественные изменения кровотока отмечены у 35 и 19 больных соответственно. Показатели кровотока подтвердили наличие у обследованных хронической абдоминальной ишемии.
Известно, что степень функциональных и морфологических нарушений толстой кишки, ассоциированных с ишемией, варьируется в больших пределах [5, 7, 9–14]. Это подтвердили результаты ирригоскопии (у 21 больного) и колоноскопии (у 20 пациентов). У 18 больных был снижен или, наоборот, повышен тонус толстой кишки, отмечалась недостаточность баугиниевой заслонки. У 19 обследованных выявлены единичные или множественные дивертикулы, у 13 – полипы от 0,2 до 0,5 см, располагавшиеся в левых отделах толстой кишки. При колоноскопии у двух больных обнаружены очаги гиперемии, у четырех пациентов – эрозии в сигмовидной кишке.
У больных с выраженными качественными и количественными нарушениями кровотока дивертикулы, полипы и эрозивно-воспалительные изменения наблюдались в основном в левых отделах толстой кишки. У них также выявлялись по два-три сосудистых, гемодинамически значимых поражения ЧС, ОПА и СА. У каждого третьего больного наблюдались качественные и количественные признаки нарушений кровотока по ВБА.
Биопсия выполнена 23 больным. Биоптаты получали из области селезеночного угла (n = 8), средней трети сигмовидной кишки (n = 4) и ректосигмоидного изгиба (n = 11).
У 21 из 23 обследованных при гистологическом исследовании обнаружены дистрофические изменения эпителиоцитов и бокаловидных клеток, у четырех из них – острые эрозии.
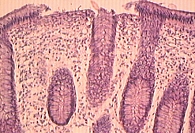
У большинства пациентов отмечены отек собственной пластинки и ее инфильтрация плазматическими клетками и лимфоцитами с примесью эозинофилов. У двух пациентов выявлены лимфатические фолликулы в собственной пластинке, у одного – гиперпластический полип. У 16 больных обнаружены микроциркуляторные нарушения: атония сосудов, стазы эритроцитов, тромбы различного происхождения, деструкция сосудов с экстравазатами эритроцитов, запустевание сосудов микроциркуляторного русла, лимфоцитарная инфильтрация собственной пластинки тонкой кишки (рис. 1). У двоих обследованных слизистая оболочка толстой кишки была неизмененной.
Таким образом, практически у всех больных с клиническими симптомами МИК в слизистой оболочке сигмовидной кишки обнаружены признаки нарушения микроциркуляции и воспаления, характерные для ишемического поражения.
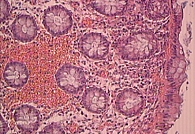
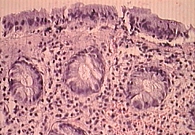
Микроскопические признаки ишемии появились еще до макроскопических. При гистологическом исследовании слизистой оболочки отмечались поверхностный некроз эпителия, уменьшение числа бокаловидных клеток, очаговые лимфоидноклеточные инфильтраты, парез и полнокровие (рис. 1–3). Эти изменения сопровождались запустеванием сосудов, развитием стазов, тромбозов микроциркуляторного русла и плазморрагиями.
Описанные морфологические изменения слизистой оболочки сигмовидной кишки, выявленные с помощью биопсии, мы отнесли к наиболее ранним достоверным признакам МИК.
У всех больных проведенные исследования позволили предположить наличие МИК.
Абдоминальный болевой синдром был связан с хронической абдоминальной ишемией. Об этом свидетельствуют отсутствие точечной локализации боли и разный ее характер. В свою очередь это косвенно может указывать на полиорганность ишемии. У большинства пациентов боль преимущественно локализовалась в проекции левого отдела толстой кишки. Не менее весомым признаком абдоминальной ишемии было появление боли после еды или физической нагрузки. Сосудистое происхождение этих симптомов подтверждалось прежде всего аускультативными, пальпаторными и инструментальными методами исследования – соответствующие признаки поражения брюшного отдела аорты, чревного ствола и брыжеечных артерий.
Исходя из результатов проведенного обследования, мы предположили наличие связи между болью и нарушением функции кишечника, с одной стороны, и ИПТК – с другой. В то же время инструментальные исследования кишечника не всегда подтверждали этот вывод. Так, при рентгенологическом исследовании толстой кишки ни у одного из обследованных не было обнаружено классических признаков ишемического колита. Речь, в частности, идет о дефектах наполнения в виде «отпечатка большого пальца», мелкозубчатых контурах толстой кишки вследствие отека, кровоизлиянии и атрофии слизистой оболочки, стенозе и язвенно-деструктивных изменениях слизистой толстой кишки.
Ряд авторов описывают три формы ишемического колита: транзиторную, стенозирующую (псевдотуморозную) и гангренозную [4–6]. Среди 52 лишь у двух больных с эрозивно-воспалительными поражениями сигмовидной кишки можно было заподозрить транзиторную форму ИПТК. У остальных пациентов макроскопических признаков деструктивных изменений кишечника (в виде язв, стенозов и т.д.) не было отмечено. При этом гистологическое исследование подтвердило наличие у них воспалительно-дистрофических, атрофических и микроциркуляторных поражений слизистой оболочки. Ишемическая природа патогистологических изменений не вызывала сомнений, поскольку язвенный колит, болезнь Крона и другие воспалительные заболевания толстой кишки были исключены.
На основании полученных данных мы выделили еще одну форму ИПТК – микроскопическую. По аналогии с известным микроскопическим (лимфоцитарным и коллагеновым) колитом она получила название «микроскопический ишемический колит». Данная форма ИПТК развивается у больных, страдающих МС, ожирением, СД 2 типа, заболеваниями сердечно-сосудистой системы.
Итак, клиническими симптомами МИК являются боли в животе разного характера с преобладанием в левой подвздошной области, возникающие или усиливающиеся после еды. Как правило, у больных нарушен стул. Чаще преобладают запоры, что объясняется ухудшением пропульсивной функции толстой кишки. В результате появляются дискомфорт в животе и метеоризм. Характерным объективным симптомом служит боль при пальпации ободочной кишки. Сигмовидная кишка чаще спазмирована и наиболее болезненна. Слепая кишка обычно расширена, ее пальпация сопровождается шумом в виде плеска воды (симптом Образцова).
Лечение
При МИК применяют консервативные методы лечения. В первую очередь это гиполипидемическая диета: 10–15% белков, 25–30% жиров, 55–60% углеводов полисахаридного ряда. Жиры должны быть исключительно растительного происхождения, продукты питания – содержать много клетчатки. Пища принимается дробно, малыми порциями. При назначении диеты необходимо учитывать индивидуальные особенности пациентов, в том числе наличие сопутствующих заболеваний.
Для нормализации уровня липидов также назначают гиполипидемические препараты. Их выбор обусловлен индивидуальной переносимостью. Возможно использование препаратов из группы статинов: симвастатина, аторвастатина. При недостаточном гиполипидемическом эффекте статинов к терапии можно добавить ингибиторы абсорбции холестерина в кишечнике (эзетимиб). Курс лечения длится от полутора до трех месяцев под контролем биохимических показателей крови.
В целях коррекции липидного спектра крови больным с сопутствующими заболеваниями печени (стеатозом, стеатогепатитом, фиброзом) в качестве альтернативы рекомендуют препараты урсодезоксихолевой кислоты, а также эссенциальные фосфолипиды.
Для улучшения реологических свойств крови используют препараты из группы низкомолекулярных гепаринов, в частности надропарин кальция в дозе 0,3 мл один раз в сутки в течение двух месяцев.
С целью антиоксидантной защиты применяют препарат триметазидина дигидрохлорид 20 мг три раза в сутки во время еды в течение трех месяцев два раза в год, а также оксиметилэтилпиридина сукцинат 100 мг в/в капельно один раз в сутки в течение двух недель.
Пациентам с сопутствующими АГ и ИБС с целью нормализации артериального давления и дилатации коронарных сосудов, а также улучшения перфузии внутренних органов назначают препараты нитрогруппы – изосорбида динитрат 10 мг три раза в день (максимально 20 мг четыре раза в день), бета-адреноблокаторы – атенолол 50–100 мг/сут, метопролол 100 мг/сут, ингибиторы ангиотензинпревращающего фермента – Моноприл 10 мг два раза в день (максимально 20 мг два раза в день) длительно, блокаторы кальциевых каналов – верапамил 40 мг три раза в день (максимально 80 мг три раза в день), амлодипин 10 мг/сут.
Для устранения симптомов диспепсии показаны ферментные препараты – Креон в дозе 10 000 ЕД два-три раза в день или 25 000 ЕД в день (при необходимости возможен прием и большей дозы, например две-три капсулы).
Необходимым и обязательным условием успешной терапии МИК является санация толстой кишки. Это позволяет не только купировать болевой синдром, проявления кишечной диспепсии, но и уменьшить эндотоксикоз. В последние годы предпочтение отдается более современному и безопасному антибиотику рифаксимину.
Рифаксимин воздействует на большинство грамположительных и грамотрицательных как аэробных, так и анаэробных бактерий. Препарат практически не всасывается в желудочно-кишечном тракте. При пероральном приеме натощак в крови обнаруживается не более 0,4% принятой дозы.
Минимальное всасывание вещества в плазму крови снижает риск развития системных побочных эффектов, внекишечных лекарственных взаимодействий. Кроме того, это позволяет не корректировать дозу у пациентов с заболеваниями печени и почек.
Рекомендованная схема приема: 800–1200 мг/сут (две таблетки по 200 мг два-три раза в день) в течение семи – десяти дней.
После курса санирующей терапии необходимо применение пребиотиков и пробиотиков, кишечных прокинетиков, миотропных спазмолитиков.
Целесообразно назначение мебеверина. Препарат устраняет спазм гладких мышц кишки, но не вызывает гипотонию, что очень важно при лечении пожилых пациентов.
Для уменьшения выраженности метеоризма можно порекомендовать комбинированный препарат альверина цитрат и симетикон (Метеоспазмил). Схема применения: по одной капсуле два-три раза в день.
Препаратом выбора для лечения запоров у пожилых больных, лиц с СД 2 типа, МС, заболеваниями печени является Мукофальк®. Это единственный препарат на основе пищевых волокон, зарегистрированный в России. Препарат не только является уникальным источником пищевых волокон. Он обладает послабляющим/антидиарейным (в зависимости от дозы), гиполипидемическим, а также пребиотическим действием.
Мукофальк® выпускается в форме гранул для приготовления суспензии.
В состав препарата Мукофальк® входят гидрофильные волокна наружной оболочки семян подорожника овального. Из всех видов растительных объем-формирующих растворимых волокон семена подорожника овального в наибольшей степени способны абсорбировать воду. Гидрофильные пищевые волокна из оболочки семян не расщепляются ферментами тонкой кишки, поэтому достигают толстой кишки в неизмененном виде, где и оказывают свое воздействие. Псиллиум главным образом состоит из углеводов (> 90%) и небольшого количества растительных белков (3–4%), минеральных и других компонентов (3–4%). Основной действующий компонент – слизеподобный гидроколлоид арабиноксилан, характеризующийся крайне высокими показателями набухания и удержания воды.
Терапевтические эффекты Мукофалька объясняются уникальным сочетанием разных фракций пищевых волокон: A, B, C.
Фракция А – нерастворимая в щелочной среде и неферментируемая бактериями. По сути, она является балластным веществом, которое нормализует моторику кишечника, влияет на осмотическое давление, притягивает жидкость в просвет кишки и формирует объем кишечного содержимого.
Фракция В – активная гельформирующая, частично ферментируемая фракция. Она отвечает за послабляющее действие препарата. За счет нее увеличивается объем содержимого кишечника, размягчаются каловые массы, обеспечивается физиологическая смазка стенки кишечника, гиполипидемический эффект, закрепляющее действие при диарее.
Фракция С – быстроферментируемая фракция. Благодаря ей замедляется постпрандиальная эвакуация из желудка. Кроме того, она обладает выраженными пребиотическими свойствами. Стимулирует рост бифидо- и лактобактерий и образование короткоцепочечных жирных кислот, которые являются основным источником энергии для эпителия толстой кишки.
Мукофальк® показан:
- при хроническом запоре (в том числе при беременности и после родов);
- синдроме раздраженного кишечника;
- дивертикулярной болезни;
- геморрое и трещинах анального прохода;
- диарее (поддерживающая терапия);
- дислипидемии;
- язвенном колите и болезни Крона;
- дисбиозе кишечника;
- комплексной терапии ожирения;
- в послеоперационный период (для размягчения консистенции кала).
Назначают Мукофальк® по одному пакетику или одной чайной ложке два – шесть раз в день. Перед употреблением гранулы высыпают в стакан, который медленно наполняют холодной водой (150 мл), размешивают и тотчас выпивают, затем запивают еще одним стаканом жидкости.
При повышенном уровне холестерина (от легкой до умеренной степени) Мукофальк® рекомендуется принимать во время еды. В этом случае препарат следует смешивать с достаточным количеством воды, фруктового сока или подобных жидкостей (не менее 150 мл). После перемешивания полученную суспензию выпивают, затем принимают дополнительную жидкость того же объема.
Заключение
Одним из проявлений патологического состояния толстой кишки у больных МС считается микроскопический ишемический колит. К его характерным симптомам относятся боль в животе с преобладанием в левой подвздошной области, возникающая после еды, запоры, дискомфорт в животе и метеоризм. При осмотре сигмовидная кишка болезненная, спазмированная, слепая – чаще расширенная, симптом Образцова. Патогистологическими признаками МИК являются некрозы поверхностного эпителия, уменьшение числа бокаловидных клеток, очаговые лимфоидно-клеточные инфильтраты и микроциркуляторные нарушения с развитием стазов, тромбозов и плазморрагий в собственной пластинке слизистой оболочки толстой кишки.
При МИК используются консервативные методы лечения, как немедикаментозные (гиполипидемическая диета), так и медикаментозные, целью применения которых является купирование или уменьшение боли, выраженности диспепсических явлений, снижение уровня липидов плазмы крови, улучшение гемодинамических показателей и показателей тканевого метаболизма.
В комплексной терапии МИК особое место принадлежит Мукофальку. Препарат обладает уникальными свойствами. Он не только регулирует моторику кишечника, но и обладает гиполипидемическим и выраженным пребиотическим действием.
L.A. Zvenigorodskaya, A.M. Mkrtumyan
A.S. Loginov Moscow Clinic Scientific Center
A.I. Evdokimov Moscow State University of Medicine and Dentistry
Contact person: Larisa Arsentyevna Zvenigorodskaya, msll@rambler.ru
Metabolic syndrome (MS) is the recognized risk factor for the development of the cardiovascular system diseases, as well as the predictor of their more severe course and terrible outcomes. At the same time, the risk of digestive disorders in MS is being often underestimated by clinicians. That is why, as a rule, such are diagnosed in the later stages.
However, in patients with MS, changes in the colon are being detected in 58.5% of cases and have clinical and morphological signs of micro ischemic colitis (MIC). Microscopic ischemic colitis is a form of circulatory-hypoxic intestinal damage and is characterized by structural changes in the mucosa and other layers of the colon.
The pathogenesis of MIC is being conditioned by a number of factors, among which of importance are: the violation of the microcirculation of the colon mucous membrane, dysbiotic disorders and motor disorders of the colon. In MS, the main definitions of which are abdominal obesity and insulin resistance, the prerequisites for the implementation of these pathogenetic mechanisms are created.
The article describes the features of the MIC course, the criteria of its diagnosis and treatment approaches.
