Цитологическая диагностика мукоэпидермоидного рака легкого
- Аннотация
- Статья
- Ссылки
- English
Введение
Мукоэпидермоидный рак бронха – редкая опухоль, подобная опухоли сиалоцитарного происхождения и характеризующаяся наличием клеток, вырабатывающих слизь и кератин, и клеток промежуточного типа. Мукоэпидермоидную опухоль с двойным метапластическим потенциалом P. Masson и L. Berger (1924) первоначально обнаpужили в слюнной железе. Были выявлены как доброкачественные опухоли, так и опухоли, склонные к рецидивированию и метастазированию. H. Smetana и соавт. (1952) описали такие же опухоли, исходящие из клеточных элементов бронхиальных желез. Эти новообразования длительный период времени относили к аденомам бронхов. Однако выяснилось, что они ведут себя как злокачественные новообразования [1, 2]. Последние годы для их обозначения используется термин «мукоэпидермоидный рак».
Мукоэпидермоидные опухоли составляют около 2% злокачественных опухолей нижних дыхательных путей и 6% (3–9%) опухолей трахеобронхиальных желез.
Патология встречается у лиц от девяти до 78 лет. Средний возраст больных – 34,8 года. Однако около 50% пациентов моложе 30 лет. Соотношение заболевших мужчин и женщин оценивается как 9:1.
К 1980 г. описано более 80 случаев мукоэпидермоидного рака дыхательных путей (пять на 1000 случаев бронхогенного рака), 51 из них у детей [3].
Мукоэпидермоидный рак трахеи впервые был описан P.E. Larson и соавт. (1965), затем G.P. Trentini и соавт. (1970) и H. Said и соавт. (1988). Анализируя собственные наблюдения, исследователи отметили, что в трахее элементы данной опухоли чаще встречаются в сочетании с другими гистологическими структурами. Мукоэпидермоидный рак трахеи в чистом виде описали N.K. Leonardi и соавт. (1978).
В настоящее время известны 12 задокументированных случаев мукоэпидермоидного рака трахеи, в том числе три случая у детей [9]. Среди отечественных исследователей впервые об этой локализации опухоли упомянул К.Ф. Юдаев [4].
Мукоэпидермоидная опухоль имеет вид эндофитного или экзофитного образования диаметром от 0,8 до 6,0 см. Располагается, как правило, на задней/боковой стенке бронха или на границе с главным бронхом и покрыта слизистой оболочкой [5]. Микроскопически паренхима опухоли с высокой степенью дифференцировки состоит из железистых структур, трубочек, кист и солидных комплексов. Железистый компонент доминирует более чем в половине случаев. Призматические муцинозные элементы, бокаловидные клетки или светлые кубические онкоцитарные клетки выстилают железы или кисты. Кисты могут разрываться, в результате слизь попадает в окружающую строму и создаются условия для гранулематозного процесса. Кроме того, выявляются базальные и промежуточные (транзиторные) клетки, реже – кератиноциты, формирующие солидные очаги, гнезда и тяжи. Полигональные клетки промежуточного типа имеют центрально расположенные ядра и амфофильную или слабоэозинофильную цитоплазму. Ороговевающие клетки с эозинофильной или прозрачной цитоплазмой обладают межклеточными мостиками, однако роговых жемчужин не формируют. Строма обычно гиалинизирована и может напоминать амилоид. В ней отмечаются очаги обызвествления или окостенения.
До 80% случаев наблюдений представлены низкодифференцированной формой мукоэпидермоидного рака, при которой описанные выше признаки двухфазной специализации опухолевой паренхимы сглажены. Кроме того, при данной форме рака клеточный полиморфизм и митотическая активность опухолевой паренхимы выражены сильнее. Примерно у половины больных отмечаются признаки инвазии в легочной паренхиме [5–7].
По цитологической картине отличить мукоэпидермоидный рак от умеренно дифференцированной аденокарциномы практически невозможно. Опухоль можно распознать при исследовании отпечатков с биоптата. В данном случае цитологическая картина будет иметь следующие особенности: элементы базального, реже – шиповатого слоя эпидермиса образуют массивные скопления, присутствуют секретирующие слизь опухолевые клетки, встречаются также элементы с железистой дифференцировкой в виде отдельных клеток, клеточных групп и железистоподобных структур. Размеры и форма железистых клеток варьируются в зависимости от количества слизи в цитоплазме. В мазках иногда обнаруживаются группы опухолевых клеток с вакуолизированной или пенистой цитоплазмой. Их наличие особенно характерно для мукоэпидермоидного рака.
К клиническим признакам относятся раздражение или обструкции дыхательных путей (кашель, кровохарканье, лихорадка), а также пневмония или ателектаз. Примерно у четверти пациентов клиническая симптоматика отсутствует [7–9].
Клинический случай
Нами проведена морфологическая диагностика мукоэпидермоидного рака у пациента В. 39 лет. Больной был направлен в стационар с диагнозом «правосторонняя внебольничная пневмония».
Из анамнеза известно, что в течение месяца пациент жаловался на сухой кашель, усиливающийся в положении лежа на спине и на правом боку, повышение температуры тела – максимально до 38,5 ºС в вечернее время.
При поступлении выполнена компьютерная томография органов грудной клетки и головного мозга: двусторонний гидроторакс, справа осумкованный, в перикарде выпот, объемные образования головного мозга и отек головного мозга в стадии компенсации. Осложнение основного заболевания – угроза тампонады сердца.
В тот же день проведены пункция плевральной полости слева, перикарда и дренирование перикарда. Из плевральной полости эвакуировано около 800 мл экссудата, из перикарда – 300 мл.
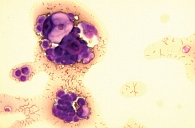
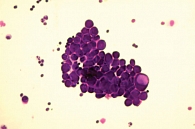
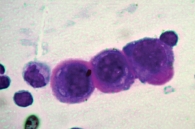
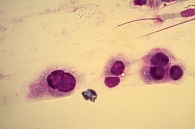
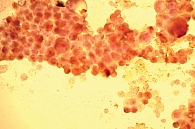
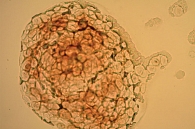
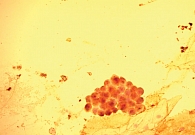
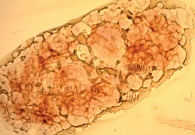
При цитологическом исследовании осадка выпотной жидкости обнаружены элементы злокачественной опухоли, имеющие сходство с аденокарциномой. Поэтому были взяты мокрота, мазки-отпечатки и браш-биопсия правого легкого (бронх первого порядка, нижний и средний долевой бронх). В материалах выявлены злокачественные клетки с центрально расположенными ядрами и эозинофильной цитоплазмой, некоторые с признаками секреции (рис. 1–4).
Гистогенез опухоли был неясен, поэтому было проведено иммуноцитохимическое (ИЦХ) исследование с использованием панели антител: TTF-1, СК7, СК5/6, р63, р53, MUC-1. В клетках опухоли не наблюдалось экспрессии TTF-1, однако окраска на CK5/6, p63, р53, MUC-1 дала резко положительный результат, в 40% клеток опухоли положительная реакция на СК7 (рис. 5–8).
Исходя из клинических проявлений заболевания и результатов цитологического и ИЦХ-исследований, сделано заключение: иммунофенотип опухоли соответствует мукоэпидермоидному раку легкого.
Результаты гистологического исследования материала биопсии: в стенке бронха множественные очаги опухолевого роста, состоящие из гнезд и тяжей атипичных крупных клеток с полиморфными гиперхромными ядрами, множественными патологическими митозами.
Результаты иммуногистохимического исследования: СК7, p63, Ki67 – экспрессия положительная, TTF-1, CD56, CgA – реакция отрицательная. Иммунофенотип опухоли соответствует плоскоклеточному раку. Индекс пролиферации 50%.
Заключение: низкодифференцированный плоскоклеточный рак (G3).
В описанном клиническом случае имела место сложная в диагностическом плане морфологическая картина. В экссудате, полученном из полости перикарда, обнаружены клетки злокачественной опухоли эпителиальной природы. Морфологический диагноз цитопатологом установлен с помощью дополнительного метода исследования – иммунофенотипирования опухоли. На основании результатов ИЦХ-исследования предоперационно установлен диагноз – мукоэпидермоидный рак, метастатическое поражение перикардиальной и плевральной полостей.
Заключение
При наличии железистого и плоскоклеточного компонентов в традиционных цитологических препаратах, приготовленных из биологического материала, необходимо проводить комплексное морфологическое исследование с использованием жидкостной цитологии, клеточных блоков и иммунофенотипирование. Определение гистогенеза опухоли и ее органной принадлежности позволяет значительно повысить точность цитологической диагностики.
K.S. Pavlyuk, M.G. Leonov, O.V. Gospirovitch, Ye.A. Terman
Research Institute – Regional Clinical Hospital № 1 named after Professor S.V. Ochapovsky, Krasnodar
Oncology Center № 3, Novorossiysk
Contact person: Mikhail Genrikhovitch Leonov, novonko@yandex.ru
The importance of complex morphological study using liquid cytology, cell blocks and immunophenotyping for verification of ‘mucoepidermoid lung cancer’ diagnosis was demonstrated on a specific example.
