Взаимосвязь нарушений сна и головной боли
- Аннотация
- Статья
- Ссылки
- English
Нарушениями сна страдает более 45% населения на земном шаре, и в последние десятилетия они стали глобальной проблемой здравоохранения [1].
Связь сна и головной боли хорошо известна: недостаточность сна может выступить триггером очередного приступа, а хороший сон может купировать боль. Еще в 1853 г. M. Romberg предположил, что «приступ (мигрени) обычно заканчивается глубоким и освежающим сном» [2]. А в 1873 г. E. Living высказал мнение, что «легче всего прекратить приступ мигрени, погрузившись в сон» [3].
В Международной классификации головной боли третьего пересмотра (МКГБ-3, 2018) сон упоминается 38 раз [4], а головная боль указывается в Международной классификации нарушений сна среди симптомов расстройств сна [5]. Головную боль, связанную со сном, Американская академия медицины сна называет одной из характерных жалоб при головной боли (мигрени или другого типа).
Нейроанатомические структуры, обеспечивающие болевую перцепцию и сон
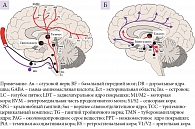
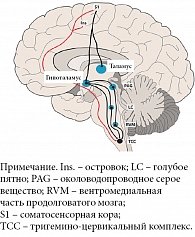
Изучение патофизиологии и функции гипоталамуса одновременно при головной боли и расстройствах сна может объяснить связь между восприятием боли с участием тройничного нерва и индукцией сна. Тригемино-цервикальный комплекс, играющий важную роль в формировании головной боли, соединен с целым рядом стволовых структур. Ноцицептивная информация поступает в ядра таламуса, активация которого имеет большое значение в развитии мигрени и кластерной головной боли. Тройничный нерв отправляет афферентные импульсы в интра- и экстракраниальные структуры и кровеносные сосуды, спинальный тригемино-цервикальный комплекс (рис. 1А) [6]. В модуляции сенсорной тригеминальной активации важны такие вазоактивные вещества, как кальцитонин-ген-связанный пептид и субстанция P. Вторичные нейроны тригеминальной системы посылают восходящие импульсы к таламокортикальным нейронам. Кроме того, существуют прямые и непрямые связи с околоводопроводным серым веществом и гипоталамусом. Третий таламокортикальный нейрон в свою очередь имеет синаптическую связь с корой, в том числе моторной, соматосенсорной и зрительной. Моноаминергические нейроны, в частности норадренергические, серотонинергические, дофаминергические, и околоводопроводное серое вещество воздействуют на таламус (орексин) и базальный передний мозг. Таким образом при развитии головной боли передается возбуждение (рис. 1Б). Тригемино-васкулярный комплекс получает прямые и непрямые модулирующие импульсы: прямые идут из соматосенсорной коры и островка, а непрямые – из гипоталамуса. Этот комплекс обеспечивает про- и антиноцицептивное взаимодействия (рис. 2). Супрахиазматическое ядро гипоталамуса получает прямые импульсы от клеток ретинального ганглия и непрямые сигналы от окружающей среды (свет – тьма). Задние нейроны таламуса получают световые сигналы с сетчатки, эти нейроны проецируют на сенсорную и зрительную кору, что является нейрональным субстратом для развития фотофобии во время приступа мигрени и повышенной чувствительности к свету (см. рис. 1Б). Моноаминергическое ядро тормозит вентролатеральное преоптическое ядро, что ведет к стимуляции гипоталамической (орексинергической) системы и ядра моста. При переходе ко сну орексинергическая система активирует вентролатеральное преоптическое ядро. Прямое торможение системы и снижение орексинергической поддержки состояния сна определяют быстрые переходы от сна к бодрствованию и наоборот. Орексинергическая система, включающая нейропептиды (орексин А и В), представлена в заднем, латеральном и паравентрикулярном гипоталамусе [7]. Орексиновые рецепторы располагаются в префронтальной коре, таламусе и подкорковых областях и участвуют в модуляции ноцицептивной нейротранс-миссии, терморегуляции, нейроэндокринных и вегетативных функциях [8]. Эти зоны задействованы и в модуляции ноцицептивной активации тригемино-васкулярного комплекса [9].
Перед приступом мигрени пациенты часто зевают, испытывают голод и чувствуют сонливость, что может быть вызвано изменениями в гипоталамусе и орексиновых нейронах и подтверждается при нейровизуализационных исследованиях с использованием функциональной магнитно-резонансной томографии до и во время приступов мигрени [10]. Таким образом осуществляется связь между системами, регулирующими процессы сна и бодрствования, и системами, участвующими в формировании головной боли.
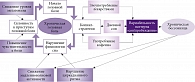
Была предложена биоповеденческая модель механизмов связи хронической инсомнии и хронической головной боли, которая предполагает три базисных пункта:
- попытки преодоления головной боли могут ускорять и усиливать нарушения сна;
- нарушение физиологии сна увеличивает склонность к головной боли;
- со временем эти циклы взаимодействуют и служат для преобразования или перехода эпизодической головной боли в хроническую (рис. 3) [11].
Среди важных предпосылок отмечены черты тревожной личности, склонность к активации симпатической нервной системы, что вместе с психологическим стрессом может быть триггером расстройств сна. Усилия по преодолению расстройств сна (компенсаторный дневной сон, прием снотворных медикаментозных препаратов перед сном и кофеина в дневное время) приводят к закреплению хронической инсомнии. Данная модель объясняет взаимодействие между биологическими и психологическими факторами развития расстройств сна [11].
Коморбидность расстройств сна и различных вариантов головной боли
Согласно МКГБ-3 (2018), различают:
- первичные головные боли, которые не являются результатом какого-либо заболевания;
- вторичные, или симптоматические головные боли, при которых боль – симптом основного заболевания;
- краниальные невралгии и другие лицевые боли;
- боли вследствие психиатрических расстройств.
Группа первичных головных болей включает мигрень, головную боль напряжения, кластерную головную боль и другие, более редкие варианты. Первичные головные боли более распространены в популяции – на них приходится 85–90% всех случаев головной боли. Именно первичные головные боли, например мигрень и кластерная головная боль, чаще сопровождаются нарушениями сна.
Связь головной боли и нарушений сна многогранна. С одной стороны, головные боли могут быть следствием нарушений сна, типичный пример – гипническая головная боль. Пациенты с мигренью и тригеминальными автономными цефалгиями, к которым относится кластерная головная боль, отмечают приступы головной боли во время сна. С другой стороны, инсомния может обусловливать развитие головной боли. В популяционных исследованиях выявлена коморбидность мигрени и синдрома беспокойных ног, мигрени и нарколепсии.
Еще один аспект – некоторые препараты, используемые для лечения головной боли, могут становиться причиной нарушений сна. Бета-блокаторы, которые входят в первую линию профилактической терапии частых приступов мигрени, вызывают тяжелые сновидения и частые ночные пробуждения. Они снижают секрецию эндогенного мелатонина, что приводит к подавлению сигнала ко сну и может вызвать нарушения сна и его фрагментацию. Так, по данным полисомнографии, было показано увеличение пробуждений на фоне приема пропранолола по сравнению с плацебо. Трициклические антидепрессанты (амитриптилин), применяемые в терапии частых приступов мигрени, не только снижают общую продолжительность сна, но и увеличивают утреннюю и дневную сонливость. Триптаны – селективные специализированные препараты для купирования приступов мигрени входят в стандарты и рекомендации по лечению мигрени. Частая сонливость может быть одним из побочных эффектов данной группы препаратов, что, по-видимому, является результатом прямого воздействия на серотонинергическую систему. Бензодиазепины, назначаемые при нарушениях сна, могут не только усиливать головную боль, но и быть причиной ее возникновения. Головная боль из-за злоупотребления лекарственными средствами усиливается при назначении препаратов, действующих на центральную нервную систему. Напротив, при профилактическом лечении мигрени антиконвульсантами (топираматом и вальпроатами) прежде всего улучшается сон, что дает первый быстрый эффект – уменьшение интенсивности и частоты приступов мигрени [12].
В Дании проведено первое масштабное эпидемиологическое исследование, которое оценивало частоту коморбидности головной боли и нарушений сна [13]. В опросе участвовали 68 518 человек, большинство из которых были моложе 55 лет (80% отвечали на вопросы офлайн, 20% – онлайн). 18,1% человек сообщили о наличии головной боли и инсомнии одновременно (высокая частота коморбидности этих заболеваний обусловлена общими патофизиологическими механизмами). Еще 16,3% страдали только от головной боли, а 21,1% имели только проблемы со сном. Коморбидная патология чаще наблюдалась у женщин и лиц среднего возраста. Среди факторов риска также отмечались низкий уровень социально-экономического статуса, нездоровый образ жизни (лишний вес/ожирение), высокий уровень стресса, тревога и депрессия. Исследователи сделали вывод о необходимости активного выявления в клинической практике пациентов с головной болью и нарушениями сна. Изменение образа жизни, снижение влияния стресса, скрининг на депрессию и тревогу могут иметь большое значение для лечения и профилактики сочетания головной боли и нарушений сна [14].
Из всех видов головной боли внимание ученых прежде всего привлекает мигрень как заболевание, значительно ухудшающее трудоспособность [13]. Частота мигрени в популяции – 14,5%. Головная боль при мигрени обычно носит пульсирующий односторонний характер, реже бывает двусторонней. Мигрени часто сопутствуют тошнота, фото- и фонофобия. Женщины страдают мигренью чаще, чем мужчины, в соотношении 5:2.
Хронобиологический паттерн мигрени был показан в многочисленных работах. Так, проспективное исследование хронобиологии мигрени (n = 1698) установило, что более половины приступов возникало с 04:00 до 09:00 часов [15].
У пациентов с мигренью нарушения сна могут быть не только триггерами приступов (в 49,8% случаев) [16], но и фактором хронизации заболевания.
По результатам исследования, посвященного анализу связи мигрени и нарушений сна, у 60,5% из 1750 пациентов, страдающих мигренью, выявлены различные варианты нарушений сна: короткая продолжительность сна, длительное засыпание, дневная сонливость, плохое качество сна, применение снотворных [17].
В другом исследовании, посвященном связи мигрени и нарушений сна, приняли участие 33 пациента с мигренью (15 с мигренью сна и 18 с обычной мигренью) [18]. Пациенты с мигренью сна чаще просыпались ночью, а у пациентов с обычной мигренью была выше частота медленноволнового сна и коротких пробуждений.
В данном исследовании, как и в ряде предыдущих, у пациентов с мигренью чаще, чем у больных контрольной группы, наблюдались симптомы тревоги. Интересно отметить, что пациенты с мигренью сна уставали днем больше, чем пациенты с обычной мигренью. Есть предположение, что низкая «возбудимость» пациентов с мигренью сна может быть связана с околоводопроводным серым веществом, структуры которого играют значимую роль в патогенезе мигрени [19].
Пациенты с мигренью чаще жалуются на бессонницу, дневную сонливость, обструктивное апноэ сна. Есть и обратная сторона – нарушения сна и уменьшение его продолжительности могут быть триггерами приступов боли. Для уточнения связи продолжительности сна и частоты приступов мигрени было проведено исследование в Южной Корее [20]. В нем приняли участие 2695 человек в возрасте 19–69 лет, из них 143 (5,3%) страдали от мигрени. Короткая продолжительность сна и плохое его качество наблюдались у 47,6% пациентов. У пациентов с мигренью распространенность сна плохого качества была статистически выше, чем в популяции. По результатам исследования отмечено, что при короткой продолжительности и плохом качестве сна приступы мигрени развивались в два раза чаще. Интенсивность головной боли не отличалась у пациентов с мигренью с коротким сном и низким качеством сна. Однако у пациентов с мигренью чаще, чем в популяции, встречались тревога (30,1 и 13,2% соответственно), депрессия (16,8 и 5,9% соответственно) и бессонница (37,8 и 9,2% соответственно).
Статистический анализ показал, что наиболее важным и независимым фактором учащения приступов мигрени была именно продолжительность сна. Полученные данные позволяют предположить, что изменение длительности сна откроет новые перспективы в лечении пациентов с мигренью [21].
Другой вид первичной головной боли – кластерная головная боль, наиболее частая среди тригеминальных автономных цефалгий. Она характеризуется выраженной односторонней головной болью и сопровождается вегетативными синдромами: покраснением глаз/лица, слезотечением, ринореей, заложенностью носа. Боль захватывает лобно-височную область и зону глазницы, обычно достигает 10 баллов по Визуальной аналоговой шкале и носит мучительный для пациента характер. Ей сопутствуют не только вегетативные симптомы в лицевой области, но и возбуждение, ажитация. Кластерная головная боль встречается в 0,1% популяции и чаще у мужчин, чем у женщин, в соотношении 4:1. Важная особенность заболевания – серии приступов головной боли с длительным межприступным периодом [22]. Кластерную боль от других головных болей отличает четкая связь атак с циркадианным ритмом. Более 75% приступов как эпизодической, так и хронической кластерной головной боли начинаются между 21:00 и 10:00 часами, как правило между 05:00 и 07:00 часами. Кластерная головная боль у шести больных из десяти сопровождается обструктивным апноэ сна, и в ряде случаев в результате лечения апноэ достигается ремиссия этой головной боли.
Проведен ряд исследований связи кластерной головной боли и секреции гормонов: мелатонина, кортизола, тестостерона, лютеинизирующего и фолликулостимулирующего гормонов, пролактина, гормона роста, тиреотропного гормона и бета-липопротеина. При кластерной головной боли концентрация большинства из них изменяется только во время приступа. Снижение уровня мелатонина в моче у пациентов с кластерной головной болью установлено именно во время серии атак головной боли. По результатам нейровизуализации, в том числе позитронной эмиссионной и функциональной магнитно-резонансной томографии, во время приступа регистрируется нейрональная активация гипоталамуса, который тесно связан с секрецией этих веществ, на стороне головной боли. С учетом полученных данных необходимо дальше изучать возможность активного использования мелатонина в лечении кластерной головной боли.
Еще один достаточно редкий вариант первичной головной боли – гипническая. Она развивается только в период ночного сна, впервые появляется после 50 лет и прогрессирует с возрастом. Большинство пациентов отмечают единичный эпизод головной боли, который возникает в середине или второй половине сна и приводит к пробуждению. В исследовании с участием 255 пациентов с гипнической головной болью у большинства развивались приступы длительностью более двух часов, начинающиеся с двух до четырех часов утра в одно и то же время.
Патофизиологические причины возникновения гипнической головной боли до сих пор не известны. Полисомнография не выявила никаких особенностей. Целый ряд исследований посвящен медикаментозному лечению гипнической головной боли с использованием лития, кофеина и индометацина.
Мелатонин в дозе 3–5 мг/сут, который применяется в лечении хронобиологических расстройств, был предложен в качестве метода лечения при гипнической головной боли и показал высокий позитивный результат [23]. Полученные данные свидетельствуют о необходимости дополнительно изучать возможность применения мелатонина при головной боли, имея в виду не только его снотворный эффект, но и противоболевое, антиноцицептивное действие.
В отличие от эпизодической хроническая головная боль значительно влияет на качество жизни и становится причиной нетрудоспособности пациентов. Хроническая головная боль отмечена у 3–5% в популяции и у 70–80% пациентов, обращающихся в центры по лечению головной боли. Надо отметить, что в МКГБ-3 под хронической головной болью понимается не длительность состояния, а количество приступов в месяц. К хроническим мигрени и головной боли напряжения относятся головная боль, приступы которой развиваются 15 и более дней в месяц на протяжении трех и более месяцев и имеют типичные для мигрени и головной боли напряжения диагностические критерии. В исследованиях по мигрени и головной боли напряжения установлена связь между головной болью и жалобами на различные расстройства сна и укорочение продолжительности ночного сна. Эта связь более выражена при хронических головных болях, нежели чем при эпизодических. Данные полисомнографии подтверждают сокращение продолжительности сна среди пациентов с мигренью и головной болью напряжения. Кроме того, были выявлены нарушение фаз медленного сна и быстрого сна при мигрени, изменение бета-ритма по результатам электроэнцефалографии в ночное время перед приступом мигрени, сопровождающееся снижением кортикальной активности [18].
Ученые из Норвегии изучали дневную сонливость как при хронической мигрени, так и при хронической головной боли напряжения [24]. Из 30 000 человек в возрасте 30–44 лет 935 пациентов, страдающих частой головной болью, были опрошены специалистами по головной боли. В итоге было выделено 405 пациентов с хронической головной болью (мигренью и головной болью напряжения), 328 (81%) из них имели дневную сонливость. Получен ряд интересных результатов. Так, отсутствовали различия между пациентами с хронической мигренью и головной болью напряжения. Дневная сонливость чаще отмечалась у пациентов с высокой частотой приступов головной боли (более 80 приступов за три месяца). Не установлена связь между результатами изменений нетрудоспособности по Шкале оценки влияния мигрени на повседневную активность, злоупотреблением лекарственными средствами и дневной сонливостью. Авторы сделали вывод о необходимости активного обнаружения нарушений сна у пациентов с хронической головной болью и одновременного лечения обоих состояний для повышения эффективности терапии и улучшения ее результатов.
Нарушения циркадианного ритма – важная составляющая в портрете пациента, страдающего не только хронической головной болью, но и депрессией. В оригинальном исследовании оценивалась связь между географическими координатами и распространенностью зимней депрессии в РФ. Проанализировано состояние 3435 подростков (1517 юношей и 1918 девушек) от 10 до 20 лет. Позднее засыпание и позднее вставание, уменьшение общей длительности сна, низкое качество сна ассоциировались с зимней депрессией у подростков обоего пола. Среди факторов, которые повышали вероятность развития зимней депрессии, были пол (выше у девушек в 1,87 раза), возраст, широта (выше на севере в 1,49 раза), часовой пояс (выше на западной границе пояса в 1,61 раза) [25].
Интересны результаты исследования связи головной боли с нарушениями сна при определенных условиях труда, включающих сменный график, напряжение и стрессы. В нем приняли участие 1102 медсестры из различных отделений трех госпиталей. Качество сна оценивали по Питтсбургскому индексу качества сна. Диагнозы (мигрень, головная боль напряжения, хроническая ежедневная головная боль) ставились на основе бета-версии МКГБ-3 (2013). Нарушения сна выявлены у 56,7% медсестер, в 34,1% случаев отмечена коморбидность нарушений сна и головной боли. У женщин с ежедневной головной болью нарушения сна встречались в 82,1% случаев. При мигрени нарушения сна наблюдались в 78,9% случаев, головная боль напряжения сочеталась с плохим качеством сна в 59% случаев [26].
Мелатонин в коррекции нарушений сна и головной боли
При обсуждении взаимосвязи нарушений сна и головной боли нельзя не отметить роль циркадианного ритма, вовлеченного в регуляцию режима сна – бодрствования. На циркадианный ритм влияет мелатонин – нейрогормон, продуцируемый преимущественно шишковидной железой и регулируемый супрахиазматическим ядром. Мелатонин играет решающую роль в регулировании циркадианных ритмов, включая инициацию сна и поддержание его ритмов. Секреция мелатонина подвержена суточному циклу – она усиливается в темное время суток и подавляется в присутствии света, процесс регулируется посредством супрахиазматических ядер гипоталамуса. Как правило, приступы мигрени возникают ранним утром, что подтверждает связь мигрени с циркадианным ритмом. Проведен ряд исследований значения мелатонина у пациентов, страдающих головной болью. Так, изучались возможность использования мелатонина как потенциально противовоспалительного вещества, его влияние на свободные радикалы и синтез цитокинов, его помощь в стабилизации мембран, модуляции серотонина и др.
Получены данные о снижении уровня мелатонина у пациентов с мигренью с аурой и без ауры, причем как в крови, так и в моче. Если у пациентов помимо мигрени отмечалась депрессия, то дефицит мелатонина был значительно больше. Показано уменьшение выраженности болевого синдрома при приеме мелатонина у пациентов с мигренью [27]. Применение мелатонина в течение трех месяцев у пациентов с нарушениями сна и коморбидной головной болью позволило уменьшить интенсивность и частоту приступов головной боли [28]. В пилотном исследовании взрослые пациенты, страдающие мигренью и головной болью напряжения, принимали мелатонин в дозе 4 мг. Из 49 включенных в исследование пациентов 41 окончил шестимесячную фазу лечения. Оказалось, что после шестимесячного лечения мелатонином частота приступов головной боли и уровень влияния головной боли на качество жизни статистически достоверно снизились по сравнению с исходным уровнем [29].
Мелаксен® («Юнифарм Инк») – препарат мелатонина в дозе 3 мг используется для нормализации циркадианного ритма. Препарат успешно регулирует цикл «сон – бодрствование», способствует нормализации ночного сна (ускоряет засыпание, снижает число ночных пробуждений, улучшает качество сна и самочувствие после утреннего пробуждения, не вызывает ощущения вялости, разбитости и усталости при пробуждении, что важно для работающих пациентов). Высказывается предположение о собственном антиноцицептивном эффекте мелатонина, который реализуется через ряд нейротрансмиттерных систем и взаимодействие с собственными мелатониновыми рецепторами. В клиническом исследовании был продемонстрирован анальгетический эффект Мелаксена при лечении боли в спине [30]. С учетом воздействия на нормализацию циркадианного ритма и улучшение продолжительности сна Мелаксен может применяться у пациентов с различными вариантами головной боли (мигренью, кластерной головной болью, гипнической головной болью) как дополнительное средство медикаментозной терапии. Использование мелатонина в качестве профилактического средства при лечении частых приступов мигрени получило экспериментальное подтверждение в двойном слепом рандомизированном исследовании. Эффективность мелатонина превосходила плацебо и амитриптилин в снижении количества приступов мигрени на протяжении трех месяцев терапии [31].
Таким образом, проведенные исследования позволили накопить достаточно большой материал, свидетельствующий о взаимосвязи различных нарушений сна и головной боли, общих патофизиологических и психологических причинах развития этих состояний. Полученные данные позволяют применять мелатонин не только для нормализации циркадианного ритма и лечения нарушений сна, но и в комплексной терапии головной боли, особенно хронической.
Заключение
Развитие новых медикаментозных стратегий, воздействующих на таргетные специфические рецепторы, может дать новое понимание одновременно механизмов регуляции сна и связи между системами сна и бодрствования и системами, генерирующими головную боль. Новые молекулы, действующие на контрольные цели (орексиновые рецепторы, кальцитонин-ген-связанный пептид и 5-HT1F-рецепторы), должны изучаться на предмет одновременного влияния как на нарушения сна, так и на головную боль.
Публикация поддержана компанией «Юнифарм Инк» (США).
M.I. Koreshkina
Scandinavia Clinic, Saint Petersburg
Contact person: Marina Igorevna Koreshkina, koreshkina-mi@avaclinic.ru
The article deals with the pathophysiological and behavioral mechanisms of the relationships between disordered sleep and headache. Particular attention is paid to the effect of sleep disorders in primary headaches – migraine and cluster headache. The article presents data the use of melatonin in complex treatment of chronic headaches.
