Эра ингибиторов в медицине: все ли нам известно? VIII Национальный конгресс эндокринологов «Персонализированная медицина и практическое здравоохранение». Сателлитный симпозиум компании MSD
- Аннотация
- Статья
- Ссылки




Роль ингибиторов дипептидилпептидазы 4 в управлении сахарным диабетом 2 типа с позиций патогенеза
Согласно данным экспертов Международной федерации диабета, увеличение распространенности сахарного диабета (СД) сопровождается повышением частоты тяжелых осложнений и летальных исходов. Так, по причине СД ежегодно умирает около 5 млн пациентов. Заведующий кафедрой эндокринологии Российской медицинской академии непрерывного профессионального образования, заслуженный деятель науки РФ, д.м.н., профессор Александр Сергеевич АМЕТОВ особо подчеркнул, что эти грозные данные в наибольшей степени обусловливают актуальность рассматриваемой проблемы и применения современных стратегий в управлении диабетом.
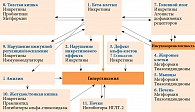
Сегодня общепризнанной считается β-клеточно-ориентированная модель развития СД 2 типа. Снижение функции и массы β-клеток поджелудочной железы сопровождается снижением секреции инсулина. Принципиально важное значение имеет инсулинорезистентность, развивающаяся вследствие усиления липолиза в жировой ткани, снижения утилизации глюкозы мышцами и увеличения продукции глюкозы печенью. К известным на сегодняшний день 11 звеньям патогенеза СД 2 типа следует также отнести дисфункцию α-клеток, нейромедиаторов головного мозга, нарушение микрофлоры кишечника с возможным снижением секреции глюкагоноподобного пептида 1 (ГПП-1), хроническое системное воспаление, связанное с нарушением иммунорегуляции и жирового метаболизма, увеличение скорости абсорбции глюкозы в желудке/тонком кишечнике и скорости реабсорбции глюкозы почками.
Гипергликемия в 90% случаев сопровождается глюкозотоксичностью, нарушением жирового обмена, повышением уровня свободных жирных кислот и липотоксичностью. Острая глюкозотоксичность запускает окислительный стресс, стресс эндоплазматического ретикулума, что в свою очередь ведет к дальнейшему снижению функции β-клеток.
Установлено, что с течением времени здоровые β-клетки теряют пластичность, способность реагировать на изменяющиеся потребности организма в инсулине, то есть демонстрируют метаболическую негибкость. В дальнейшем может наблюдаться апоптоз β-клеток либо их дифференцировка и приобретение функций α-клеток. Вместо инсулина они начинают производить глюкагон с последующим снижением инкретинового эффекта.
«Уменьшение функции и массы β-клеток приводит к уменьшению секреции инсулина, снижению инкретинового эффекта, нарушению функции α-клеток, повышенной секреции глюкагона, что способствует повышенному выбросу глюкозы печенью и формированию гипергликемии. Это целая цепочка центральных событий, в основе которых лежит снижение сигналов со стороны ГПП-1», – отметил выступающий.
Большую часть патофизиологических проблем можно решить с помощью продления действия эндогенного ГПП-1. Предотвратить его быстрый распад можно путем ингибирования ферментативной активности дипептидилпептидазы 4 (ДПП-4). Установлено, что ингибиторы ДПП-4 и агонисты рецепторов ГПП-1 оказывают воздействие на семь из 11 звеньев патогенеза СД 2 типа (с первого по третий и с седьмого по десятый), еще на три дефекта (с четвертого по шестой) – метформин и тиазолидиндионы, на 11-й дефект – ингибиторы натрий-глюкозного котранспортера 2 (НГЛТ-2) (рис. 1)1.
По мнению профессора А.С. Аметова, при выборе оптимального сахароснижающего препарата для конкретного пациента с СД 2 типа необходимо учитывать не только его гликемические эффекты, но и негликемические. Речь, в частности, идет о влиянии на массу тела, сердечно-сосудистый риск, плейотропные эффекты. Все имеет значение: и профиль безопасности лекарственного средства, и его переносимость, и удобство применения. «Иначе повреждение клеток, органов и тканей может достичь точки невозврата. Тогда не останется никаких шансов на восстановление нормальных соотношений между глюкагоном и инсулином», – уточнил выступающий.
Ингибиторы ДПП-4 препятствуют быстрому распаду ГПП-1, что позволяет восстановить его физиологические концентрации, а также концентрации других пептидов. Принципиально важно, что воздействие ингибиторов ДПП-4 на секрецию инсулина и глюкагона носит глюкозозависимый характер. Кроме того, данный класс препаратов обладает широким спектром плейотропных эффектов.
По словам докладчика, ситаглиптин – один из первых ингибиторов ДПП-4, который он и его коллеги стали применять в клинической практике в комбинации с метформином.
Далее докладчик предcтавил результаты исследования, проведенного с целью оценить влияние комбинированной терапии ситаглиптином и метформином на показатели жирового обмена у пациентов с СД 2 типа и избыточным весом2.
В исследование были включены 82 пациента с СД 2 типа, не достигшие целевых уровней гликированного гемоглобина (HbA1c) на монотерапии метформином (HbA1c > 6,5%). Помимо СД 2 типа у них отмечались избыточная масса тела (ожирение), нарушение липидного обмена. Первую группу составили 42 пациента, ранее получавших монотерапию метформином в дозе 1500–2000 мг/сут и переведенных на комбинированную терапию ситаглиптином 100 мг/сут с метформином 2000 мг/сут. Во вторую группу вошли 40 пациентов, ранее находившихся на диетотерапии. Им была назначена монотерапия метформином в дозе 2000 мг/сут.
После формирования клинических групп все пациенты прошли клинико-инструментальное и лабораторное обследование. У них также определяли антропометрические показатели (рост, вес, индекс массы тела (ИМТ), окружность талии (ОТ) и бедер и их соотношение), показатели углеводного обмена (глюкоза плазмы натощак (ГПН), постпрандиальная гликемия (ППГ), HbA1c), а также проинсулина, инсулина, С-пептида в крови. Кроме того, у них оценивали показатели жирового обмена (липидный профиль, содержание адипонектина, лептина). Функциональную активность β-клеток поджелудочной железы определяли с помощью индекса НОМА-β, инсулинорезистентность – НОМА-IR. Для оценки количества и характера распределения жировой ткани использовали магнитно-резонансную томографию (МРТ).
Через 24 недели на фоне комбинированной терапии ситаглиптином и метформином у больных СД 2 типа и ожирением наблюдалось достоверное снижение уровня гликемии натощак, постпрандиальной гликемии, гликированного гемоглобина.
Уровень ГПН в среднем снизился на 2,67 ммоль/л, ППГ – на 3,26 ммоль/л, HbA1c – на 1,63%. Количество достигших целевого уровня HbA1c < 7% было наибольшим в группе комбинированной терапии (69,05%).
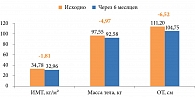
Через шесть месяцев в первой группе отмечалось достоверное снижение ИМТ – в среднем на 1,8 кг/м2, массы тела – на 4,97 кг (рис. 2).
Одновременно со снижением массы тела наблюдалось выраженное уменьшение окружности талии – в среднем на 6,5 см. Уменьшение окружности талии, а также соотношения окружности талии к окружности бедер на 0,03 см в первой группе указывает на снижение висцерального жира, а значит, на снижение инсулинорезистентности.
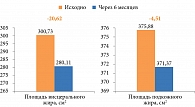
Результаты повторной МРТ подтвердили благоприятное перераспределение жира. В частности, в первой группе площадь висцерального жира в среднем уменьшилась на 20,62 см2, подкожного жира – на 4,51 см2 (рис. 3).
На фоне терапии ситаглиптином и метформином отмечалось более выраженное снижение уровня лептина (на 30,4%) и более выраженное повышение содержания адипонектина (на 27%).
Кроме того, терапия ситаглиптином в комбинации с метформином сопровождалась улучшением липидного профиля.
Улучшение гликемического контроля происходило на фоне достоверного снижения инсулинорезистентности, соотношения проинсулина к инсулину, уменьшения индекса HOMA-IR и повышения индекса НОМА-β. По мнению профессора А.С. Аметова, это можно расценить как положительное влияние на функцию β-клеток поджелудочной железы за счет уменьшения глюкозотоксичности и липотоксичности.
Таким образом, комбинация ситаглиптина и метформина позволяет добиться выраженного улучшения показателей гликемического контроля и жирового обмена у больных СД 2 типа и избыточной массой тела, не достигших целевых значений гликемии на фоне монотерапии метформином.
Препарат Янумет Лонг представляет собой фиксированную комбинацию ситаглиптина и метформина пролонгированного высвобождения. Комплементарное действие двух компонентов препарата Янумет Лонг и прием один раз в сутки позволяют положительно влиять не только на углеводный обмен, но и на приверженность терапии.
Завершая выступление, профессор А.С. Аметов призвал коллег преодолевать клиническую инерцию для лучшего управления диабетом.
«Долой клиническую инерцию – ранняя интенсификация, лечение до цели, пожизненное обучение пациентов и членов их семей», – подчеркнул он в заключение.
Ингибирование дипептидилпептидазы 4 при сахарном диабете 2 типа: почему это важно
По словам заведующего отделением диабетической стопы Национального медицинского исследовательского центра эндокринологии (НМИЦ эндокринологии), д.м.н., профессора Гагика Радиковича ГАЛСТЯНА, наступившая в медицине эра ингибирования ознаменована разработкой и производством все новых классов препаратов, позволяющих целенаправленно, точечно воздействовать на те или иные нарушения в организме. Примером тому могут служить ингибиторы ДПП-4, благодаря которым можно селективно влиять на ДПП-4 и, соответственно, на целый ряд механизмов регуляции метаболизма глюкозы.
Сначала исследовали классические механизмы ингибирования ДПП-4 – в плазме, следствием которых является повышение активности ГПП-1 в плазме. Однако позднее были открыты и неклассические механизмы, в частности в кишечнике, в островках Лангерганса, в тканях3. Ингибирование ДПП-4 в кишечнике позволяет повысить уровень ГПП-1 в портальной системе и кишечнике. Это способствует увеличению активности автономной нервной системы, которая тоже регулирует функцию β-клеток, и уменьшению продукции глюкозы печенью. Ингибирование ДПП-4 в островках поджелудочной железы снижает деградацию ГПП-1 в β-клетках. За счет этого увеличивается секреция инсулина, уменьшается секреция глюкагона и воспаление. Ингибирование ДПП-4 в тканях предупреждает деградацию других пептидов, которые являются субстратами для ДПП-4. Речь прежде всего идет о таком важном инкретиновом гормоне, как глюкозозависимый инсулинотропный полипептид (ГИП), а также о стромальном клеточном факторе 1α (SDF-1α). Ингибирование ДПП-4 позволяет повысить экспрессию SDF-1α, который целенаправленно воздействует на механизмы окислительного стресса, воспаление, реабсорбцию натрия, что может влиять на прогноз не только в отношении функции почек, но и других осложнений диабета4.
Последние исследования возможных натрийуретических механизмов ингибиторов ДПП-4 свидетельствуют, что транспорт натрия на фоне их применения происходит в иных отделах извитых канальцев, чем при использовании ингибиторов НГЛТ-2 или агонистов рецепторов ГПП-15. Однако пока ни одно исследование не подтвердило снижение конечных почечных точек при применении ингибиторов ДПП-4. По мнению профессора Г.Р. Галстяна, для того чтобы увидеть разницу, нужно проводить долгосрочные наблюдения.
В последние годы выявлена еще одна причина развития диабетической ретинопатии. В основе ее развития помимо сосудистых поражений лежит дегенерация сетчатки6. Данные изменения возникают за несколько лет до постановки диагноза при проведении офтальмоскопии. Повышение активности ГПП-1 может играть важную роль в упреждении развития данного патологического процесса, что требует дальнейшего изучения.
Определенные перспективы связаны с подавлением повышенной экспрессии ДПП-4 и влиянием на репарацию при раневых процессах на фоне СД 2 типа, что также активно изучается7. Таким образом, плейотропные эффекты ингибиторов ДПП-4 могут распространяться не только на β-клетки, регуляцию метаболизма глюкозы, но и на ряд других процессов.
Далее профессор Г.Р. Галстян представил клинический случай. Пациентка, 76 лет. Страдает СД 2 типа 18 лет, HbA1c – 7,8%, скорость клубочковой фильтрации – 48 мл/мин/1,73 м². Госпитализирована в отделение диабетической стопы НМИЦ эндокринологии с нейроишемической формой синдрома диабетической стопы, критической ишемией правой нижней конечности.
Из анамнеза: инфаркт миокарда два года назад, одна гипогликемическая кома три года назад, симптоматически подтвержденные гипогликемии два-три раза в месяц. Пациентка получала следующую терапию: ингибиторы ангиотензинпревращающего фермента, β-блокаторы, статины, антитромботики, инсулин гларгин 28 ЕД, гликлазид 90 мг, метформин 1000 мг.
По словам докладчика, у пациентки отмечены семь из девяти факторов, ассоциированных с повышенным риском гипогликемий, одним из которых является прием препаратов инсулина и сульфонилмочевины.
Для данной больной чрезвычайно важно упредить гипогликемические эпизоды, особенно тяжелые. В то же время отменить инсулинотерапию нельзя, поэтому необходимо найти инсулину безопасного «партнера».
Наиболее оптимальным, по мнению профессора Г.Р. Галстяна, является ингибитор ДПП-4. Глюкагонотропный эффект позволяет восстановить чувствительность α-клеток к глюкозе, что делает инсулинотерапию более безопасной, без ускользания эффекта в отношении гликемии8–10.
Есть ли подтверждение этому? В исследовании CompoSIT-I была реализована концепция продолжения терапии ингибитором ДПП-4 ситаглиптином (Янувия) у пациентов с СД 2 типа на фоне инициации базальной инсулинотерапии11. В него было включено 743 пациента. Средний возраст больных – 58 лет. Длительность диабета – более десяти лет. Уровень HbA1c – 8,8%.
Участников исследования разделили на две группы. Первая (n = 373) получала комбинацию ситаглиптина и инсулина гларгин, вторая (n = 370) – плацебо и инсулин гларгин.
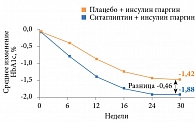
Через 30 недель терапии в группе «ситаглиптин + инсулин гларгин» отмечалось большее снижение уровня HbA1c по сравнению с группой «плацебо + инсулин гларгин» – -1,88 против -1,42% (рис. 4). Разница в среднем изменении уровня HbA1c составила -0,46% (при 95%-ном доверительном интервале (ДИ) -0,58 – -0,34, р < 0,001).
Доля пациентов с симптоматической гипогликемией была сопоставима в обеих группах – 33,5% в группе «ситаглиптин + инсулин гларгин» и 37,7% в группе «плацебо + инсулин гларгин».
В целом группы были сопоставимы по частоте нежелательных явлений, в том числе в отношении динамики массы тела.
«Таким образом, результаты исследования продемонстрировали целесообразность продолжения применения ситаглиптина на фоне инициации базальной инсулинотерапии у больных СД 2 типа», – констатировал профессор Г.Р. Галстян.
Нерешенные вопросы комплексного подхода к терапии сахарного диабета 2 типа
Заведующая кафедрой эндокринологии Первого Московского государственного медицинского университета им. И.М. Сеченова, д.м.н., профессор Нина Александровна ПЕТУНИНА сфокусировала свое выступление на эффективных подходах к решению таких важных проблем, как трудность достижения целей лечения, клиническая инертность и отсутствие приверженности терапии.
Согласно метаанализу 24 исследований, включавших более 369 тыс. больных СД 2 типа из 20 стран, только 42,8% из них достигали уровня HbA1c < 7% и лишь 29% имели показатели артериального давления < 130/80 мм рт. ст.12
К сожалению, приходится констатировать, что появление новых терапевтических возможностей и технологий не привело к достижению терапевтических целей у большего числа пациентов с диабетом13.
Программа «ДИА-контроль» позволила получить данные реальной клинической практики, сложившейся в области лечения СД 2 типа в крупнейших российских регионах. Они подтверждают несвоевременность интенсификации сахароснижающей терапии14. Это может быть одной из причин неудач в лечении. В формирование клинической инертности наибольший вклад (50%) вносят факторы со стороны врача (сложности при постановке диагноза, несвоевременное начало терапии, неудачи при титрации дозы и пр.). Свою лепту также вносят факторы со стороны пациента (уровень обучения, комплаентности) (30%) и системы здравоохранения (20%)15. Дело в том, что низкая приверженность пациентов лечению программирует врача на клиническую инертность. И наоборот, пациенты с высокой приверженностью, обученные, мотивированные, позволяют врачу активнее действовать и принимать решение об интенсификации лечения.
В последнем совместном консенсусе экспертов Американской диабетической ассоциации и Европейской ассоциации по изучению диабета (2018 г.) был представлен алгоритм принятия решения для пациент-ориентированного управления СД 2 типа16. Он включает не только оценку ключевых характеристик пациента, рассмотрение специфических, влияющих на терапию факторов, но и совместное принятие решений при создании и инициации плана лечения, цель которого предотвратить осложнения и улучшить качество жизни.
По словам профессора Н.А. Петуниной, стратегия ранней интенсификации терапии считается одним из способов преодоления клинической инерции.
Подтверждением могут служить результаты исследования CompoSIT-M по оценке эффективности и безопасности раннего начала терапии ситаглиптином (Янувией) на фоне повышения дозы метформина у пациентов с СД 2 типа17.
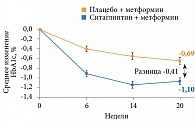
Пациенты с уровнем HbA1c ≥ 7,5% и ≤ 11,0% на терапии метформином 1000 мг/сут были рандомизированы на две группы: группу терапии ситаглиптином один раз в день в комбинации с метформином (после рандомизации осуществлялась титрация дозы до 1000 мг два раза в день) (n = 229) и группу, получавшую лечение метформином (после рандомизации титрация дозы до 1000 мг два раза в сутки) плюс плацебо (n = 229). Через 20 недель терапии в первой группе отмечалось большее снижение уровня HbA1c (-1,1%) по сравнению со второй группой (-0,69%). Разница в среднем изменении HbA1c составила -0,41% (95% ДИ -0,59– -0,23, р < 0,001) (рис. 5).
Полученные данные позволили сделать вывод, что у участников исследования, не достигших целевого уровня HbA1c на субмаксимальной дозе метформина, добавление ситаглиптина во время повышения дозы метформина улучшало гликемический ответ и достижение целевых значений HbA1c при сходной безопасности и переносимости по сравнению со стратегией повышения дозы метформина.
Еще одной причиной плохого управления диабетом является низкая приверженность лечению. Ни для кого не секрет, что весомыми факторами, влияющими на приверженность пациентов лечению, считаются переносимость и схема приема лекарственных средств. Было выявлено, что применение метформина в стандартной форме примерно в 25% случаев сопряжено с побочными эффектами со стороны желудочно-кишечного тракта (ЖКТ). В 5–10% случаев это приводило к прекращению приема препарата18. По данным исследований, метформин с пролонгированным высвобождением характеризовался меньшей частотой нежелательных явлений со стороны ЖКТ по сравнению с метформином немедленного высвобождения. Как следствие, повышалась приверженность лечению18, 19.
Стартовая терапия фиксированной комбинацией ситаглиптина и метформина характеризовалась лучшей переносимостью и меньшим количеством нежелательных явлений со стороны ЖКТ по сравнению с монотерапией метформином20. Следовательно, фиксированная комбинация ситаглиптина и пролонгированной формы метформина (препарат Янумет Лонг) потенциально может снижать частоту побочных эффектов со стороны ЖКТ и увеличивать приверженность пациентов лечению. Повышению приверженности служит и удобная схема приема препарата – один раз в день21.
На сегодняшний день совершенно четко определена патогенетическая связь между СД и патологией ЖКТ. Кроме того, ЖКТ – это мишень при сахарном диабете. Заболевания пищевода, желудка, тонкой и толстой кишки являются частой гастроэнтерологической формой диабетической автономной нейропатии.
В связи с этим особого внимания заслуживают установленные ассоциации между метаболическим синдромом, диабетом и нарушением микробиоты кишечника. Микробиота – источник энергии для хозяина. К ее основным функциям также относят стимуляцию ангиогенеза, защиту от патогенной флоры, локальный и системный иммунитет, переваривание пищи, регуляцию энтеральных нервов, развитие микроворсинок кишечника, синтез витаминов, молочной кислоты и короткоцепочечных жирных кислот22.
В исследованиях на моделях животных показано, что диета с высоким содержанием жиров вызывала дисбактериоз, изменяла функцию микробиоты кишечника23. В дальнейшем был проведен целый ряд исследований по оценке разных методов терапевтического воздействия на микробиоту. Продемонстрировано, в частности, что изменения микробиоты вследствие приема метформина могут снижать уровень глюкозы и обуславливать ряд побочных эффектов24.
Метформин снижает абсорбцию желчных кислот и глюкозы, повышает концентрацию солей желчных кислот в кишечнике, что повышает осмотический градиент, вызывая диарею, и вторично, возможно, нарушает состав микробиоты25.
Ситаглиптин в свою очередь способен оказывать протективное действие на микробиоту. В экспериментальных исследованиях на животной модели применение ситаглиптина способствовало восстановлению соотношения Firmicutes/Baсteroidetes при СД 2 типа26. Это может объяснять лучшую переносимость метформина при применении его в комбинации с ситаглиптином.
В настоящее время активно изучается взаимосвязь микробиома с когнитивными нарушениями.
Установлено, что СД 2 типа связан со значительным количеством факторов риска, которые могут влиять на когнитивные функции, – начиная с острых последствий гипер- и гипогликемии, через призму микро- и макрососудистых осложнений, артериальную гипертензию, гиперхолестеринемию, ожирение и, конечно, возраст27. Клинические, эпидемиологические и экспериментальные исследования указывают на взаимосвязь между СД и когнитивными нарушениями. Доказано, что у пациентов с СД более чем в два раза выше риск развития сосудистой деменции, в два – четыре раза – болезни Альцгеймера, в полтора – два раза – риск ускоренного возрастного снижения когнитивных функций по сравнению с лицами соответствующего возраста без диабета28.
В проспективном обсервационном исследовании оценивалось влияние Янувии (ситаглиптина) на когнитивные функции у больных СД 2 типа с или без болезни Альцгеймера29. В исследование исходно были включены 253 пожилых пациента с СД 2 типа. Их разделили на две группы. Первая группа (n = 126) получала метформин и/или инсулин, вторая группа (n = 127) – ситаглиптин 100 мг/сут плюс метформин и/или инсулин. Период исследования составил 24 недели. В начале и конце исследования проводилась оценка не только стандартных показателей (массы тела, ИМТ, гликированного гемоглобина), но и когнитивных функций. Последнее – с помощью шкалы оценки когнитивного статуса (Mini-Mental State Examination – MMSE).
Анализ динамики когнитивных функций у пациентов с СД 2 типа без болезни Альцгеймера через шесть месяцев терапии продемонстрировал более высокие показатели MMSE в группе, получавшей только ситаглиптин или инсулин, по сравнению с пациентами, получавшими только метформин (р = 0,024). Сравнение динамики когнитивных функций у пациентов с СД 2 типа и болезнью Альцгеймера проводилось в подгруппах терапии ситаглиптином и метформином, поскольку количество лиц с болезнью Альцгеймера, получавших инсулин, было очень ограничено (n = 3). Результаты свидетельствуют об улучшении показателей MMSE в группе ситаглиптина по сравнению с группой метформина через шесть месяцев применения (р = 0,047).
Таким образом, СД ассоциируется с когнитивными нарушениями, и это также может снижать приверженность лечению. Поэтому при выявлении когнитивных нарушений у больных СД 2 типа следует рассмотреть возможность назначения фиксированных комбинаций с однократным приемом.
Завершая выступление, профессор Н.А. Петунина перечислила основные мероприятия по повышению приверженности лечению больных СД 2 типа, а именно: простые схемы лечения, снижение кратности приема, применение фиксированных комбинаций, минимизация побочных эффектов, в том числе в отношении массы тела, риска гипогликемий, повышение образования и улучшение взаимодействия «врач – пациент».
Остеопороз – незамеченное осложнение сахарного диабета
Согласно определению экспертов Всемирной организации здравоохранения, остеопороз представляет собой системное заболевание скелета, характеризующееся снижением массы костей и нарушением микроархитектуры костной ткани, приводящим к повышению хрупкости костей и высокому риску их переломов. Как отметил заведующий кафедрой эндокринологии и диабетологии Московского государственного медико-стоматологического университета им. А.И. Евдокимова, руководитель отдела эндокринных и метаболических заболеваний Московского клинического научного центра им. А.С. Логинова, заслуженный врач России, д.м.н., профессор Ашот Мусаелович МКРТУМЯН, у больных сахарным диабетом высок риск развития остеопороза и в случае перелома шейки бедра большинство летальных исходов происходит в первые три – шесть месяцев после перелома, при этом 20–30% этих смертей связаны с переломом как таковым, а не с его последствиями30.
Наличие СД 2 типа, несмотря на нормальную минеральную плотность костей, ассоциируется с плохим качеством костной ткани, вследствие чего повышается хрупкость костей и риск переломов. Согласно последним данным, на хрупкость костей при СД 2 типа влияют неферментативное гликозилирование коллагена, снижение костного метаболизма, провоспалительное состояние, потеря инкретинового эффекта, жировое перерождение костного мозга, нарушение регуляции адипокинов, гипогонадизм, инсулинорезистентность, снижение уровня инсулиноподобного фактора роста 1, нарушение метаболизма кальция (Ca) и повышение уровня паратгормона (ПТГ)31, 32.
На риск переломов у больных диабетом оказывают влияние эпидемиологические факторы (возраст, пол), осложнения диабета (ретинопатия, нефропатия, нейропатия), факторы, специфические для диабета (высокий уровень HbA1c, гипогликемия, ятрогенные эффекты), и связанные с ними падения.
Практически у каждого третьего больного диабетом поражены органы-мишени (ретинопатия, нейропатия, нефропатия) и, соответственно, повышен риск переломов33. Среди больных диабетом наиболее подвержены риску переломов лица старше 50 лет34.
Мультивариантный анализ риска переломов шейки бедра в зависимости от уровня HbA1c у более 20 тыс. пожилых пациентов с СД 2 типа продемонстрировал повышение риска при уровне HbA1c > 9% и выше. Самым безопасным в этом отношении оказался уровень HbA1c в пределах 6–7%35.
В другом исследовании проводился анализ риска переломов, связанных с падением, в зависимости от наличия гипогликемии у пациентов с СД 2 типа старше 65 лет. Гипогликемии повышали риск переломов36.
Профессор А.М. Мкртумян представил собственное видение патогенеза диабетического остеопороза. В его основе лежит декомпенсация на фоне хронической гипергликемии, метаболический ацидоз, жировой гепатоз, глюкозурия, гиперкальциурия, гиперфосфатурия. Как следствие, снижается синтез D-гормона, всасывание кальция в кишечнике, развивается отрицательный баланс Са и вторичный гиперпаратиреоз, что нарушает механизм отрицательной обратной связи ПТГ-Са и усиливает резорбцию костной ткани.
Безусловно, выбор сахароснижающих препаратов должен основываться не только на их эффективности, но и на их безопасности, в том числе в отношении риска переломов. На сегодняшний день получены данные о возможном положительном влиянии ингибиторов ДПП-4 на клетки костной ткани37. Ряд других противодиабетических препаратов оказывает нейтральное влияние, при этом установлено, что некоторые препараты могут повышать риск переломов. Так, была выявлена связь между применением канаглифлозина, тиазолидиндионов и повышенным риском переломов32, 38.
По данным общенационального когортного исследования с участием 207 558 пациентов в возрасте 50 лет и старше, начавших применение противодиабетических препаратов с 2008 по 2011 г., лечение ингибиторами ДПП-4 может оказывать защитное воздействие на метаболизм костной ткани по сравнению с препаратами сульфонилмочевины при добавлении к метформину39.
В Германии был проведен ретроспективный анализ данных реальной клинической практики в отношении двух сопоставимых по возрасту, полу, продолжительности диабета групп пациентов на монотерапии метформином: в первой группе (n = 4160) пациенты когда-либо применяли ингибиторы ДПП-4, во второй группе (n = 4160) никогда не применяли ингибиторы ДПП-4. Ретроспективный анализ показал, что применение ингибиторов ДПП-4 в комбинации с метформином у пациентов с СД 2 типа было ассоциировано со снижением риска развития переломов по сравнению с монотерапией метформином40.
Резюмируя сказанное, профессор А.М. Мкртумян подчеркнул, что остеопороз является недооцененным или незамеченным осложнением СД 2 типа, которое требует ранней диагностики. При выборе сахароснижающей терапии следует отдавать предпочтение препаратам, безопасным в отношении риска переломов. Согласно результатам рандомизированных исследований и анализа данных пациентов с СД 2 типа, ситаглиптин не повышает риск переломов.
Заключение
Одна из главных проблем в управлении диабетом заключается в клинической инерции, причинами которой могут выступать риск развития гипогликемий, увеличение массы тела, сложные схемы лечения, отсутствие приверженности терапии. Представленные экспертами результаты рандомизированных клинических исследований и клинической практики убедительно доказывают, что своевременная интенсификация лечения ситаглиптином или фиксированной комбинацией ситаглиптина и метформина обеспечивает воздействие практически на все звенья патогенеза СД 2 типа, способствуя устойчивому гликемическому контролю с минимальным риском гипогликемий. Комплементарное действие двух компонентов препарата Янумет Лонг и прием один раз в сутки позволяют не только положительно влиять на углеводный обмен на фоне лучшей переносимости, но и повышать приверженность пациентов лечению19, 21.
