LAUREL: ретроспективная программа по применению инсулина гларгин (Лантус®) для лечения пациентов с СД типа 2 в повседневной клинической практике
- Аннотация
- Статья
- Ссылки


Это связано как с увеличением количества больных за счет прогнозируемого резкого роста заболеваемости в развивающихся странах и увеличения продолжительности жизни в индустриально-развитых странах, так и с преждевременной инвалидизацией и смертностью пациентов в связи с развитием поздних осложнений СД (5, 7, 12, 16, 15). Уже в настоящее время СД типа 2 является тяжелым бременем для экономики даже индустриально-развитых стран: затраты на лечение больных СД типа 2 в 2-3 раза выше, чем у лиц без этого заболевания, и растут по мере ухудшения гликемического контроля и прогрессирования осложнений (1, 6).
Результаты исследования UKPDS убедительно продемонстрировали необходимость интенсивного гликемического контроля у пациентов с СД типа 2 с целью профилактики развития и прогрессирования микро- и макроваскулярных осложнений СД (14). В принятом в 2006 г. совместно ADA и EASD Консенсусе по ведению пациентов с СД типа 2 рекомендовано снижение уровня HbА1с как можно ближе к норме (< 6%) при условии отсутствия гипогликемических состояний, при этом целесообразно раннее начало и своевременная интенсификация инсулинотерапии (9).
В настоящее время на рынке имеется как минимум три препарата инсулина пролонгированного действия: уже ставший классическим НПХ-инсулин, а также аналоги инсулина – инсулин гларгин и инсулин детемир. Инсулин гларгин (ЛантусÒ) – это первый аналог инсулина, который появился на мировом рынке в 2000 г. и применяется для лечения больных СД в Российской Федерации с 2003 г. За это время проведено большое количество хорошо контролируемых клинических исследований, в которых оценивалась эффективность и безопасность инсулина гларгин, причем в большинстве исследований он сравнивался с НПХ-инсулином, наиболее широко применяемым для заместительной базальной терапии (3, 4, 8, 10, 11, 13, 17). Однако жесткость протоколов этих исследований создает ограничения для экстраполяции полученных таким образом результатов на повседневную клиническую практику. Более ценную информацию о применении изучаемых препаратов и их влиянии на пациентов могут обеспечить наблюдательные программы, включающие крупные когорты пациентов, применяющих эти препараты в повседневной жизни (2).
В связи с этим нами была проведена программа по применению инсулина гларгин (ЛантусÒ) у больных СД типа 2 в широкой клинической практике.
Основной целью программы была оценка и сравнение эффективности применения инсулина гларгин и НПХ-инсулина (изменение уровня HbA1c) у пациентов с СД типа 2. Также планировалось оценить и сравнить такие показатели эффективности и безопасности применения обоих инсулинов, как изменение гликемии натощак, средние дозы препаратов, частоту эпизодов гипогликемии.
Материалы и методы
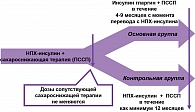
Дизайн. Многоцентровая, открытая, ретроспективная программа с использованием параллельных групп, сравнивавшая продолжение терапии НПХ-инсулином и перевод с терапии НПХ-инсулином на терапию инсулином гларгин у пациентов с СД типа 2. Программа проводилась в поликлиниках Российской Федерации при участии 366 врачей-эндокринологов (рисунок 1).
Данные о пациентах регистрировались в специально разработанных картах-опросниках. В картах регистрировалась информация о демографических и антропометрических характеристиках пациента, о проводимой сахароснижающей терапии, дозах пероральных сахароснижающих препаратов (ПССП), типе базального инсулина и его суточной дозе, уровне HbA1c и гликемии натощак, частоте и типе гипогликемий, частоте проведения самоконтроля с помощью глюкометра, количестве посещений пациентом врача и случаев неотложной госпитализации.
Характеристика пациентов. В программу были включены 1192 пациента с СД типа 2, из них 796 (276 мужчин, 520 женщин) пациентов за 4-9 месяцев до момента включения в программу были переведены с терапии НПХ-инсулином на инсулин гларгин (основная группа) и 396 (133 мужчины, 263 женщины) пациентов в течение минимум 12 месяцев до момента включения в программу получали НПХ-инсулин (контрольная группа).
Критерии включения:
- СД типа 2;
- мужчины и женщины старше 18 лет;
- для основной группы – перевод с НПХ-инсулина на инсулин гларгин за 4-9 месяцев до включения в программу при условии отсутствия изменений в сопутствующей сахароснижающей терапии;
- для контрольной группы – терапия НПХ-инсулином в течение как минимум 12 месяцев до включения в программу при условии отсутствия изменений в сопутствующей сахароснижающей терапии.
Критерии исключения:
- пациенты с СД типа 2, получающие другие, отличные от инсулина гларгин и НПХ-инсулина, инсулины среднего и длительного действия, а также смешанные инсулины;
- СД типа 1; гестационный диабет;
- беременные и кормящие женщины;
- пациенты, находящиеся на стационарном лечении;
- любые клинически значимые органные или системные заболевания, делающие невозможным интерпретацию и оценку результатов;
- для основной группы – любые изменения в сахароснижающей терапии за исключением перевода с НПХ-инсулина на инсулин гларгин;
- для контрольной группы – любые изменения в сахароснижающей терапии в течение 6 месяцев до включения пациента в программу.
Общая характеристика пациентов представлена в таблице 1.
Статистический анализ. Описательная статистика для демографических характеристик и величин HbA1c, гликемии натощак, дозы инсулина представлена в виде среднего арифметического значения и стандартного отклонения. Также использовался дисперсионный анализ повторных измерений ANOVA для оценки переменных эффективности – уровня HbA1c и гликемии натощак, дозы инсулина. В необходимых случаях параметрический анализ подтверждался непараметрическими методами. Сравнение групп по качественным признакам осуществлялось путем анализа таблиц сопряженности с использованием двустороннего точного критерия Фишера, методом χ-квадрата, при помощи метода Мантель–Хенцеля. Сравнение внутри группы по качественным признакам осуществлялось при помощи критерия Мак-Немара. Данные в тексте и в таблицах представлены в виде M ± m (M – среднее арифметическое значение, m – стандартное отклонение). Статистически значимыми считали различия при р < 0,05.
Результаты
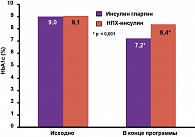
Анализ эффективности. Исходно уровень HbA1с в группе, переведенной на терапию инсулином гларгин, составлял 9,0 ± 1,6%, в группе, продолжавшей терапию НПХ-инсулином, – 9,1 ± 1,6% (p = 0,449). К концу наблюдения отмечено статистически значимое снижение уровня HbA1с как в группе, получавшей инсулин гларгин, так и в группе, получавшей НПХ-инсулин: –1,8 ± 1,40% и –0,7 ± 1,10% соответственно (р < 0,001 для обеих групп), однако уровень HbA1с в группе инсулина гларгин был статистически значимо ниже, чем в группе НПХ-инсулина (p < 0,001) (рисунок 2).
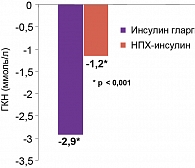
Уровень гликемии в группе, переведенной на терапию инсулином гларгин, исходно составлял 9,5 ± 2,3 ммоль/л и не отличался от уровня гликемии в группе, продолжавшей терапию НПХ-инсулином: 9,5 ± 2,3 ммоль/л (p = 0,786). К концу наблюдения отмечено статистически значимое снижение уровня гликемии в обеих группах: –2,9 ± 2,3 ммоль/л и –1,2 ± 2,1 ммоль/л соответственно (р < 0,001 для обеих групп), однако уровень гликемии в группе инсулина гларгин был ниже, чем в группе НПХ-инсулина (p < 0,001) (рисунок 3).
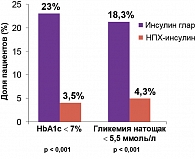
С клинической точки зрения большую значимость имеет не столько снижение уровня параметров углеводного обмена само по себе, сколько достижение целевых значений этих показателей. В связи с этим необходимо отметить, что в группе, получавшей инсулин гларгин, доля пациентов с уровнем HbA1с < 7% выросла с 14,9 до 23,0% (р < 0,001), в то время как в группе, продолжавшей терапию НПХ-инсулином, она снизилась с 13,6 до 3,5% (р = 0,039). Доля пациентов, достигших уровня гликемии < 5,5 ммоль/л, выросла с 14,1 до 18,3%, в то время как в группе пациентов, продолжавших получать НПХ-инсулин, доля пациентов с уровнем гликемии < 5,5 ммоль/л снизилась с 13,4 до 4,3% (р < 0,001) (рисунок 4).
Средние дозы базального инсулина исходно были одинаковыми в обеих группах: в группе, переведенной на инсулин гларгин, средняя доза составляла 26,8 ± 12,4 МЕ (медиана 26,0 МЕ), в группе, продолжавшей терапию НПХ-инсулином – 27,9 ± 10,6 МЕ (медиана 26,5 МЕ) (p = 0,156) (таблица 2). К концу наблюдения доза инсулина статистически значимо выросла в обеих группах до 27,9 ± 10,2 МЕ (медиана 28,0 МЕ) и 31,4 ± 10,6 МЕ (медиана 30,0 МЕ) соответственно (р < 0,001), однако была незначительно выше у пациентов, продолжавших терапию НПХ-инсулином. Изменений в дозах ПССП и прандиальных инсулинов в течение всего периода наблюдения не было.
Анализ безопасности. Мы проанализировали частоту всех типов гипогликемии в обеих группах в течение месяца перед завершением программы. В группе, получавшей инсулин гларгин, статистически значимо меньшая доля пациентов испытала симптоматически подтвержденные гипогликемии, чем в группе, получавшей НПХ-инсулин: 1 эпизод был зарегистрирован у 33 из 796 (4,1%) пациентов и 32 из 396 (8,1%) пациентов соответственно, 2 эпизода – у 12 из 796 (1,5%) пациентов и 20 из 396 (5,1%) пациентов соответственно, 3 эпизода – у 9 из 796 (1,1%) пациентов и 15 из 396 (3,8%) пациентов соответственно (p < 0,001 между группами). Также статистически меньшее количество пациентов в группе, получавшей инсулин гларгин, испытало ночные гипогликемии по сравнению с пациентами, получавшими НПХ-инсулин: 1 эпизод был зарегистрирован у 37 из 796 (4,6%) пациентов и 61 из 396 (15,4%) пациентов соответственно, 2 эпизода – у 8 из 796 (1,0%) пациентов и 54 из 396 (13,6%) пациентов соответственно, 3 эпизода – у 8 из 796 (1,0%) и 28 из 396 (7,1%) пациентов соответственно (p < 0,001 между группами). Тяжелую гипогликемию данных испытали 3 из 796 (0,4%) пациентов, получавших инсулин гларгин, и 11 из 396 (2,8%) пациентов, получавших НПХ-инсулин (p < 0,001). Вместе с этим частота экстренных госпитализаций в течение последнего месяца перед сбором данных между группами не различалась и составляла 0,5% в группе инсулина гларгин и 1,5% в группе НПХ-инсулина (р = 0,071). Также одинаковым было количество посещений пациентами обеих групп своих врачей: 42,2% в группе инсулина гларгин и 47,7% в группе НПХ-инсулина (р = 0,071).
Обсуждение результатов
В программе приняли участие 366 врачей-эндокринологов, работающих в городских муниципальных поликлиниках, которые включили в программу в общей сложности 1192 пациента с СД типа 2: на 1 врача приходилось в среднем чуть больше 3 пациентов. Это позволяет экстраполировать полученные результаты на всю популяцию пациентов с СД типа 2.
В большинстве контролируемых клинических исследований эффективность инсулина гларгин и НПХ-инсулина в достижении целевых значений HbA1c и гликемии натощак была одинаковой при существенно более низком риске развития всех типов гипогликемии на терапии инсулином гларгин. В нашей программе частота всех типов гипогликемии на терапии инсулином гларгин также была статистически значимо ниже, чем на терапии НПХ-инсулином. Вместе с этим также продемонстрировано статистически значимо большее снижение уровней HbA1c и гликемии натощак на фоне терапии инсулином гларгин по сравнению с терапией НПХ-инсулином. При этом динамика дозы и инсулина гларгин, и НПХ-инсулина в течение программы была незначительной (сопутствующая сахароснижающая терапия оставалась неизменной в течение всего периода наблюдения).
Можно предположить, что основной причиной столь выраженного улучшения состояния углеводного обмена при незначительном увеличении дозы инсулина гларгин является более низкая вариабельность гликемии в течение суток у этих пациентов по сравнению с пациентами, получавшими НПХ-инсулин. Вместе с тем нельзя не отметить, что доля пациентов, достигших целевых значений HbA1c и гликемии натощак на фоне терапии инсулином гларгин, в нашей программе значительно ниже, чем в хорошо известных клинических исследованиях – Treat-To-Target, LANMET и др. При этом в нашей программе 69,1% пациентов, получавших инсулин гларгин, и 57,3% пациентов, получавших НПХ-инсулин, измеряли уровень гликемии ежедневно. И здесь становится понятна причина большей эффективности инсулина гларгин по сравнению с НПХ-инсулином в сочетании с достаточно низким количеством пациентов, достигших компенсации углеводного обмена на фоне терапии инсулином гларгин: в обеих группах фактически не проводилась титрация дозы инсулина.
Таким образом, более низкая вариабельность гликемии в течение суток, являющаяся одним из преимуществ инсулина гларгин перед НПХ-инсулином, привела к улучшению состояния углеводного обмена. Однако абсолютно не были использованы другие преимущества препарата – наличие простого алгоритма титрации в сочетании с хорошим профилем безопасности, что позволяет активно увеличивать дозу инсулина гларгин не просто для снижения уровня HbA1c и гликемии натощак, а, что более важно с клинической точки зрения, для достижения целевых значений этих параметров.
Итак, основной разницей между контролируемыми клиническими исследованиями и реальной клинической практикой является практически полное отсутствие титрации инсулина. Таким образом, в очередной раз подтверждается факт, что мало назначить новый препарат – в нашем случае инсулин гларгин, обладающий улучшенными фармакокинетическими и фармакодинамическими свойствами, – необходимо своевременно и адекватно увеличивать его дозу. В противном случае самоконтроль становится просто бесполезным способом расходования средств, а пациенты остаются в состоянии хронической декомпенсации углеводного обмена, т.е. продолжают подвергаться риску развития и прогрессирования поздних осложнений СД. Вместе с тем нельзя не отметить существование объективных причин для этой так называемой вторичной инсулинорезистентности: учитывая растущую распространенность СД типа 2 и появление новых препаратов и схем лечения, у врачей часто не хватает времени для проведения обучения пациента при инициации инсулинотерапии и дальнейшего постоянного мониторирования эффективности лечения. Здесь можно привести результаты исследования INITIATE (Yki-Jarvinen et al.), в котором было доказано, что можно достичь одинаково эффективного контроля гликемии при начале терапии инсулином гларгин у пациентов с СД типа 2 как в группах, так и в индивидуальном порядке (18). Эти результаты представляются чрезвычайно значимыми, поскольку начало инсулинотерапии в группах занимает вдвое меньше времени, чем индивидуальная инициация, что существенно снижает нагрузку на врачей и затраты на ведение пациентов. Выходом из сложившейся ситуации является более широкое внедрение образовательных программ для обучения основным принципам и навыкам, необходимым пациентам при инсулинотерапии.
Выводы
Программа LAUREL продемонстрировала бóльшую эффективность и безопасность применения инсулина гларгин по сравнению с НПХ-инсулином у больных СД типа 2 в повседневной клинической практике: отмечено большее снижение уровня HbA1с и гликемии натощак, а также достижение целевых значений этих параметров большим количеством пациентов в группе, получавшей инсулин гларгин, при меньшей частоте всех типов гипогликемий.
