Монотерапия ибрутинибом при В-клеточной лимфоме экстранодальной маргинальной зоны
- Аннотация
- Статья
- Ссылки
- English
Введение
Обновленная версия классификации В-клеточных лимфом маргинальной зоны (ЛМЗ) Всемирной организации здравоохранения (ВОЗ) включает экстранодальные ЛМЗ, ЛМЗ селезенки с ворсинчатыми лимфоцитами или без них, узловую ЛМЗ с моноцитоидными В-клетками или без них. Указанные три группы ЛМЗ характеризуются специфическими диагностическими критериями, различными генетическими особенностями, клиническими проявлениями и подходами к лечению [1].
Подавляющее большинство орбитальных лимфом имеют В-клеточное происхождение (97%). Из них наиболее распространенным подтипом считается В-клеточная лимфома экстранодальной маргинальной зоны (59%). За ней следует диффузная крупноклеточная В-клеточная лимфома (23%), затем фолликулярная лимфома (9%) и лимфома из мантийных клеток (5%). Орбитальная лимфома – заболевание преимущественно пожилых людей. Гистопатологический подтип и клиническая стадия заболевания являются наилучшими предикторами прогноза и исхода заболевания. Лимфомы низкой степени злокачественности, такие как экстранодальная В-клеточная лимфома маргинальной зоны и фолликулярная лимфома, имеют хороший прогноз. В то же время лимфомы высокой степени злокачественности (диффузная крупноклеточная В-клеточная лимфома и лимфома из мантийных клеток) ассоциируются с плохим прогнозом [2].
Клинический случай
В мае 2019 г. пациента после лечения в офтальмологическом отделении клиники микрохирургии глаза в Красноярске, где 24 апреля ему были выполнены орбитотомия, трансконъюнктивное удаление новообразования левой орбиты, направили в Красноярский краевой клинический онкологический диспансер им. А.И. Крыжановского (КККОД). Гистологический анализ № 9195: картина подозрительна в отношении лимфомы, рекомендовано иммуногистохимическое исследование (ИГХ). По данным ИГХ, опухолевые клетки обнаруживают мономорфную мембранную экспрессию CD20. В основе предсуществовавших фолликулов определяются скопления клеток, экспрессирующих bcl6, разрозненная сеть фолликулярных дендритных клеток, экспрессирующих CD23. Интерфолликулярно распределенные Т-клетки экспрессируют CD5. Cyclin D1 экспрессирован гистиоцитами, эндотелиоцитами. Иммунофенотип соответствует нодальной В-клеточной лимфоме маргинальной зоны. В КККОД проведено комплексное обследование. Установлен диагноз: В-клеточная лимфома маргинальной зоны бульбарной конъюнктивы с прорастанием в левую орбиту III. Рекомендовано проведение полихимиотерапии и позитронно-эмиссионной томографии, совмещенной с рентгеновской компьютерной томографией (ПЭТ/КТ), с введением фтордезоксиглюкозы (ФДГ). Данные ПЭТ/КТ с ФДГ от 15 июля 2019 г. показали признаки лимфопролиферативного заболевания с метаболически активным поражением левой глазницы, шейных, надключичных лимфоузлов справа, паховых слева, мягких тканей грудной стенки, спины и бедер.
С 24 июля по 12 ноября в КККОД пациенту провели шесть курсов по схеме R-CHOP. В ноябре 2019 г. выполнено контрольное обследование для оценки динамики лечения. Результаты ПЭТ/КТ от 26 ноября 2019 г.: признаки лимфопролиферативного заболевания с полным метаболическим ответом (1 балл). Рекомендовано продолжить терапию ритуксимабом 750 мг внутривенно капельно каждые три недели. С 2 декабря 2019 г. проведено два курса монотерапии ритуксимабом 750 мг внутривенно. 27 декабря врачебным консилиумом КККОД принято решение о динамическом наблюдении.
В марте 2020 г. выполнен контрольный осмотр. ПЭТ/КТ от 11 марта: признаки лимфопролиферативного заболевания с полным метаболическим ответом (1 балл). Рекомендовано динамическое наблюдение.
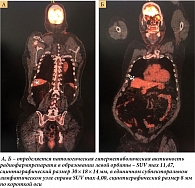
В марте 2021 г. пациент обратился в КККОД с жалобами на повышенную утомляемость. По данным мультиспиральной КТ лицевого черепа, выявлено объемное образование левой орбиты. 24 марта выполнено контрольное обследование – ПЭТ/КТ: метаболическая активность радиофармпрепарата в образовании левой орбиты, в единичном субпекторальном лимфатическом узле справа, расценена как проявление основного заболевания. По сравнению с результатами от 11 марта 2020 г. динамика отрицательная (рис. 1).
В марте 2021 г. проведена телемедицинская консультация в Национальном медицинском исследовательском центре (НМИЦ) гематологии для решения вопроса о дальнейшей тактике лечения. Рекомендованы терапия ибрутинибом 560 мг внутрь ежедневно и пересмотр гистосканов в НМИЦ гематологии. Пересмотр гистосканов проведен дважды. При первом пересмотре рекомендовано выполнить ИГХ с расширением панели антител с маркерами герминального происхождения (HGAL, CD10), ИГХ пролиферативной активности по экспрессии Ki-67, что и было сделано в КККОД. Во время второго пересмотра гистосканов в сканированных препаратах субстрата лимфомы из клеток маргинальной зоны с увеличенным количеством крупных клеток с экстранодальной локализацией данных в пользу трансформации в диффузную В-крупноклеточную лимфому не обнаружено.
С мая 2021 г. пациент получает терапию ибрутинибом 560 мг внутрь ежедневно.
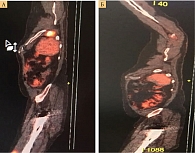
В октябре 2021 г. выполнено контрольное обследование. ПЭТ/КТ от 11 октября – без существенной динамики по сравнению с результатами от 24 марта 2021 г., DS = 4 (рис. 2).
Пациент находится под динамическим наблюдением кардиолога по месту жительства, состояние стабильное.
Электрокардиограмма (ЭКГ) от 13 октября 2021 г.: ритм синусовый, частота сердечных сокращений (ЧСС) – 57 ударов в минуту, признаки гипертрофии левого желудочка.
Эхокардиография (ЭхоКГ) от 13 октября 2021 г.: стенки аорты уплотнены, кальциноз 1-й степени кольца и створок аортального клапана, кольца митрального клапана, аневризма корня аорты (50 мм), аортальная недостаточность 2-й степени, восходящий отдел аорты расширен до 42 мм, дуга 36 мм, митральная и трикуспидальная недостаточность 1-й степени, полости левого желудочка, левого предсердия, правого предсердия расширены, стенки левого желудочка гипертрофированы, систолическая функция левого желудочка сохранена, фракция выброса по Симпсону 62%, диастолическая функция левого желудочка нарушена по первому типу, зон гипоакинезии не выявлено.
Консультация кардиолога по месту жительства 14 октября 2021 г.: абсолютных противопоказаний для проведения химиотерапии со стороны сердечно-сосудистой системы в настоящее время нет.
Терапия ибрутинибом продолжена.
В марте 2022 г. выполнен контрольный осмотр.
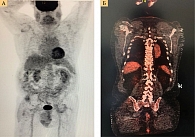
ПЭТ/КТ с ФДГ от 9 марта 2022 г.: участков патологической гиперметаболической активности не выявлено, по сравнению с данными от 11 октября 2021 г. динамика положительная (рис. 3).
В феврале 2022 г. контрольный осмотр кардиолога по месту жительства.
ЭКГ от 28 февраля 2022 г.: ритм синусовый, ЧСС – 62 удара в минуту, признаки гипертрофии левого желудочка, атриовентрикулярная блокада 1-й степени.
ЭхоКГ от 28 февраля 2022 г.: склероз аорты с аневризматическим расширением корня восходящего отдела аорты, кальциноз кольца аортального клапана, створок 1-й степени, увеличение левого предсердия, левого желудочка, симметричная гипертрофия межжелудочковой перегородки, задней стенки левого желудочка, кальциноз кольца митрального клапана, створок 1-й степени, зоны гипоакинезии не выявлено, сократительная способность левого желудочка удовлетворительная, легочная гипертензия начальная.
Консультация кардиолога по месту жительства от 28 февраля 2022 г.: абсолютных противопоказаний для проведения химиотерапии со стороны сердечно-сосудистой системы в настоящее время нет. Терапия ибрутинибом продолжена.
Обсуждение
Лимфома маргинальной зоны – это медленно развивающееся злокачественное В-клеточное заболевание крови. Заболевание отличается вялотекущим характером. Продолжительность жизни пациентов после установления диагноза может составлять несколько лет. Медиана общей выживаемости для экстранодальной ЛМЗ превышает 12 лет, для нодальной формы и ЛМЗ селезенки – 8 лет [3].
Схемы первой линии терапии ЛМЗ включают монотерапию антителами к CD20 (ритуксимаб), химиотерапию R-CHOP и комбинированную химиоиммунотерапию (ритуксимаб + бендамустин) [4]. У большинства пациентов после первой линии лечения отмечается рецидив. До настоящего времени единственным способом лечения при рецидивирующем течении заболевания оставалось повторное применение тех же препаратов. Однако кумулятивная токсичность, особенно при использовании алкилирующих препаратов, может привести к повреждению стволовых клеток, развитию миелодисплазии и острого миелолейкоза с неблагоприятным прогнозом. Расчетная частота миелодисплазии или острого миелолейкоза, связанных с лечением, варьируется от 1 до 6% в течение 20 лет наблюдения после традиционной химиотерапии.
Тирозинкиназа Брутона (ТКБ) – ключевой компонент сигнального пути рецепторов В-клеток. Генетические мутации ТКБ приводят к формированию иммунодефицита, характеризующегося отсутствием зрелых В-лимфоцитов, а именно Х-сцепленной агаммаглобулинемии (агаммаглобулинемия Брутона). Предполагалось, что ингибирование сигнального пути рецепторов В-клеток будет обладать терапевтическим эффектом при злокачественных В-клеточных заболеваниях за счет подавления миграции, пролиферации и выживаемости опухолевых клеток.
Ибрутиниб – ингибитор ТКБ (один раз в сутки) одобрен в США для лечения пациентов с ЛМЗ, которым необходима системная терапия и которые ранее получали не менее одной линии лечения на основе антител к CD20.
В многоцентровом открытом нерандомизированном исследовании II фазы PCYC-1121 (NCT01980628) оценивали эффективность и безопасность монотерапии ибрутинибом у пациентов с рецидивирующей/рефрактерной ЛМЗ. Результаты исследования II фазы PCYC-1121 применения ибрутиниба у ранее леченных пациентов с ЛМЗ продемонстрировали эффективность и безопасность монотерапии ибрутинибом у пациентов со всеми подтипами ЛМЗ (экстранодальной лимфомой лимфоидной ткани, ассоциированной со слизистыми оболочками, нодальной и ЛМЗ селезенки). PCYC-1121 – одно из самых масштабных проспективных исследований у пациентов с распространенной стадией ЛМЗ. По данным независимых экспертов, по истечении медианы наблюдения 19,4 месяца (первичный анализ) частота общего ответа (ЧОО) составила 48%. Медиана длительности ответа не была достигнута, а медиана выживаемости без прогрессирования составила 14,2 месяца. Анализ в подгруппах продемонстрировал большую частоту ответа у пациентов, ранее получавших только ритуксимаб (69%), по сравнению с теми, кто ранее получал химиоиммунотерапию на основе ритуксимаба (46%). В окончательном анализе данных исследования II фазы PCYC-1121 при медиане наблюдения 33,1 месяца (~14 дополнительных месяцах наблюдения с момента первичного анализа) монотерапия ибрутинибом продолжала ассоциироваться с достижением стойкой клинической пользы у пациентов с рецидивирующей/рефрактерной ЛМЗ. Данные исследования продемонстрировали углубление ответа в динамике: ЧОО увеличилась с 48% через год лечения до 58% через три года, а частота полного ответа – с 5% через год лечения до 10% через три года. Медиана общей выживаемости по истечении 33 месяцев наблюдения оставалась недостигнутой. Кроме того, медиана длительности устойчивого ответа составила 27,6 месяца, у 48% пациентов ответ сохранялся через 33 месяца. Новых данных о безопасности не зафиксировано. При длительности лечения ибрутинибом до 45 месяцев данные о безопасности препарата в монорежиме соответствовали данным первичного анализа и опубликованным результатам о применении ибрутиниба у пациентов с неходжкинскими лимфомами и хроническим лимфолейкозом. У всех пациентов в ходе лечения были зарегистрированы нежелательные явления (НЯ). У 45 (71%) больных зафиксированы НЯ 3-й степени тяжести и выше. К наиболее распространенным НЯ любой степени тяжести, зарегистрированным в ходе лечения, относились диарея (30 (48%) пациентов), слабость (29 (46%)), анемия (23 (37%)) и тошнота (20 (32%)). Частота самых распространенных НЯ любой степени тяжести была стабильной или снизилась в динамике. У 5 (8%) пациентов зарегистрирована фибрилляция предсердий. При этом у 3 человек эпизоды фибрилляции предсердий развились в течение первого года лечения. Во всех случаях фибрилляция предсердий была 1/2-й степени тяжести. Фибрилляция предсердий носила контролируемый характер и не потребовала коррекции дозы или прекращения приема ибрутиниба [5].
Заключение
Результаты анализа исследования PCYC-1121 демонстрируют долгосрочную безопасность и эффективность монотерапии ибрутинибом у пациентов с рецидивирующей/рефрактерной ЛМЗ.
Как показывает представленный клинический случай, монотерапия ибрутинибом позволяет достичь полного ответа независимо от типа предшествующей терапии. Это подтверждают и результаты клинического исследования.
Таким образом, данные исследования и клиническая практика свидетельствуют в поддержку применения монотерапии ибрутинибом в качестве альтернативы химиотерапии у пациентов с рецидивирующей/рефрактерной ЛМЗ при благоприятном соотношении «польза – риск» и удобной схеме приема – один раз в сутки.
Yu.V. Batukhtina, PhD, R.A. Zukov, PhD, Prof.
V.F. Voyno-Yasenetsky Krasnoyarsk State Medical University
A.I. Kryzhanovsky Krasnoyarsk Regional Clinical Oncology Dispensary
Siberian Scientific and Clinical Center of the FMBA of Russia
Contact person: Ruslan A. Zukov, zukov_rus@mail.ru
The article presents a clinical case of treatment of orbital B-cell lymphoma of the extranodal marginal zone.
This case report demonstrates the safety and efficacy of ibrutinib monotherapy in patients with relapsed/refractory LMZ previously reported in the PCYC-1121 study. Research and clinical evidence support the use of ibrutinib monotherapy as an alternative to chemotherapy in this patient population with a favorable benefit-risk profile and a convenient once-daily regimen.
