Некоторые аспекты терапии сосудистых когнитивных расстройств
- Аннотация
- Статья
- Ссылки
- English
Причины и клинические проявления когнитивных расстройств
Когнитивные нарушения – синдром, отмечающийся в популяции довольно часто, особенно в пожилом и старческом возрасте. Наиболее распространенной причиной развития когнитивных нарушений являются нейродегенеративные заболевания (как правило, болезнь Альцгеймера) и сосудистое поражение головного мозга [1–3]. Нередко у одного и того же пациента наблюдаются когнитивные расстройства как сосудистой, так и дегенеративной природы, в таком случае принято говорить о смешанных когнитивных нарушениях [4, 5].
Термин «сосудистые когнитивные расстройства» (СКР) предложил V. Hachinski [6, 7]. СКР могут быть умеренными (недементные когнитивные расстройства) и тяжелыми (деменция). В 2013 г. (когда было принято Диагностическое и статистическое руководство по психическим расстройствам 5-го пересмотра) от термина «деменция» в медицинском сообществе решили отказаться, а вместо него использовать термины «малое» (для умеренных когнитивных нарушений) и «большое» (для деменции) нейрокогнитивное расстройство. Впоследствии это нашло отражение в Международной классификации болезней 11-го пересмотра.
К факторам риска СКР относятся возраст, низкий уровень образования, недостаточная физическая активность, а также сердечно-сосудистая патология или сосудистые факторы риска: артериальная гипертензия, сахарный диабет, гиперлипидемия, перенесенный инсульт или инфаркт миокарда, абдоминальное ожирение, гиперкоагуляция, поражение сосудов иной этиологии (васкулит), нарушения ритма сердца, курение [8–10].
В основе развития СКР лежит очаговое или диффузное поражение вещества головного мозга, причинами которого могут быть атеросклероз, кардио- и артерио-артериальные эмболии, дисбаланс между артериальным притоком и венозным оттоком крови, нарушение строения и хода как крупных церебральных артерий, так и сосудов малого калибра [2, 11, 12].
К СКР может привести поражение различных отделов больших полушарий и ствола головного мозга, а конкретные клинические проявления будут зависеть от локализации сосудистых очагов. При этом на выраженность когнитивных расстройств влияют и массивность поражения вещества головного мозга, и вовлеченность в патологический процесс так называемых стратегических зон. Под стратегическими когнитивными зонами понимают отделы головного мозга, активно задействованные в познавательном процессе: подкорковые ганглии, включая таламус, гиппокамп, ствол головного мозга, лобные доли.
СКР могут развиваться:
- одномоментно после перенесенного острого нарушения мозгового кровообращения (ОНМК), поразившего достаточно большой объем головного мозга или стратегическую зону;
- постепенно со ступенеобразным нарастанием выраженности когнитивных расстройств – такой вариант типичен для мультиинфарктного поражения головного мозга или безынсультного течения СКР, когда вещество мозга поражается вследствие патологии сосудов малого калибра при артериальной гипертензии и/или сахарном диабете (болезнь малых сосудов) [6, 13].
Инсульт, безусловно, остается важнейшей причиной развития СКР. Количество перенесенных пациентом ОНМК прямо связано с выраженностью у него когнитивных расстройств. По данным большинства авторов, когнитивное снижение неизбежно при повторяющихся ОНМК, если пациенты не соблюдали назначения или им не проводилась необходимая коррекция сердечно-сосудистой патологии и сосудистых факторов риска [13–16]. Сходные результаты были получены и в ходе испытаний на базе клиники нервных болезней Первого МГМУ им. И.М. Сеченова [5].
Интересно, что предшествующие инсульту когнитивные нарушения выступают в качестве предиктора последующего постинсультного ухудшения. Так, согласно данным S. Pendlebury и соавт., среди пациентов с когнитивными нарушениями, достигшими после перенесенного ОНМК выраженности большого нейрокогнитивного расстройства, в 90% случаев снижение познавательных функций наблюдалось и до инсульта [17]. Факторами риска развития когнитивных расстройств у этих пациентов, помимо артериальной гипертензии, сахарного диабета, нарушений ритма сердца, сердечной недостаточности, были пожилой возраст, низкий уровень образования, атрофия гиппокампа и коры больших полушарий головного мозга. На основании полученных данных был сделан вывод о том, что в ряде случаев у пациентов после ОНМК когнитивные нарушения дебютируют в рамках болезни Альцгеймера. Исследования, проведенные на базе клиники нервных болезней Первого МГМУ им. И.М. Сеченова, показали, что симптомы, характерные для болезни Альцгеймера, развиваются после перенесенного ОНМК у 32% пациентов [1, 5, 11]. При сочетании СКР и типичных для болезни Альцгеймера первичных гиппокампальных нарушений памяти с прогрессирующим течением можно говорить о так называемых смешанных когнитивных нарушениях.
Важность правильной трактовки такого симптома, как нарушения памяти, при дифференциальной диагностике СКР и болезни Альцгеймера заставляет несколько подробнее остановиться на этом вопросе. При болезни Альцгеймера страдают запоминание и воспроизведение недавней информации. Пациент будет подробно рассказывать о событиях, которые имели место много лет назад, но с трудом вспоминать, что ел сегодня на завтрак, как добирался до места, где сейчас находится, что недавно смотрел или читал. Заучив информацию с исследователем, пациент сразу после этого (непосредственное воспроизведение) назовет больше слов, чем спустя некоторое короткое время (отсроченное воспроизведение). При этом роль подсказок при попытках припомнить заученный материал не существенна. У пациентов с СКР основные проблемы отмечаются при заучивании материала, но организующие методики (например, подсказки) значительно облегчают запоминание. Подобные нарушения памяти называются регуляторными и возникают в результате нарушения контроля за выполняемыми познавательными операциями. Регуляторные нарушения при СКР затрагивают не только сферу памяти, пациент будет испытывать сложности при переключении с одного вида деятельности на другой, неохотно и нелегко обучаться новым навыкам. Одновременно будут наблюдаться так называемые импульсивные симптомы: внезапный отказ от какой-либо деятельности, смена одного вида деятельности другим, резкие колебания эмоций, поведения. В некоторых случаях могут развиться двигательные расстройства: трудности при начале движения, прохождении поворотов, дверных проемов, а также постуральные нарушения, хватательные рефлексы, симптомы орального автоматизма и недержание мочи [18]. Таким образом, при СКР чаще всего поражаются подкорковые структуры, их связи с передними отделами головного мозга и непосредственно сами передние отделы головного мозга. Следует отметить, однако, что подобный тип когнитивных расстройств характерен для СКР мультиинфарктного течения или болезни малых сосудов. При когнитивных расстройствах, развивающихся в результате большого по объему инсульта, тип когнитивных нарушений будет определяться локализацией очага [19].
Проявления СКР чаще всего сочетаются с некогнитивными симптомами: флюктуирующим нарушением поведения, эмоциональным истощением, апатией, нарушениями сна. Нередко эмоционально-поведенческие расстройства дезадаптируют пациентов даже больше, чем снижение познавательных функций. Главная особенность нарушений поведения у пациентов с СКР – колебание их выраженности. В частности, может наблюдаться спонтанное ухудшение поведения с яркими проявлениями агрессии, раздражительностью, неправильной оценкой действий окружающих и собственных действий, после чего произойдет такое же внезапное, спонтанное возвращение к нормальному поведению. Подобное течение поведенческих расстройств при СКР обусловлено колебанием уровня внимания. Если при достаточном уровне бодрствования и внимания поведение пациента будет неизмененным, он будет хорошо выполнять нейропсихологические тесты, то при ослаблении произвольного контроля за деятельностью выраженность эмоциональных и поведенческих расстройств резко возрастет.
Среди симптомов, существенно ухудшающих качество жизни пациентов с СКР, нужно выделить депрессию и апатию. При депрессии пациенты часто не жалуются на плохое настроение. На первый план выходят снижение активности, апатия, инертность, безразличие, в том числе к собственному состоянию [6, 20]. Сочетание депрессии, апатии, нарушений поведения и когнитивных расстройств, несомненно, прогностически неблагоприятно, поскольку пациенты невнимательно относятся к назначениям врача, не выполняют их, не соблюдают рекомендации в отношении доз и частоты приема лекарственных средств, что в свою очередь может привести к последующим нарушениям мозгового кровообращения [21, 22].
Постановка диагноза деменции на клиническом примере
Пациентка А., 78 лет. Консультируется амбулаторно по настоянию родственников. Пациентка сообщает об эпизодических головных болях и шуме в голове. В остальном, по ее мнению, она здорова, визит к врачу считает лишним. К родственникам настроена негативно. В течение последнего года находится с ними в постоянном конфликте. Уверена, что они к ней придираются, ждут ее смерти, а пока хотят установить ей психиатрический диагноз и определить на постоянное проживание в специализированный стационар, чтобы завладеть ее имуществом.
Со слов родственников, у больной отмечаются нарушения поведения, эмоционального состояния, снижение познавательной активности, а также трудности в повседневном самообслуживании. Прогрессирующее нарушение поведения пациентки родственники наблюдают в течение последних трех лет. Она стала апатичной, большую часть времени ничего не делает, лежит или спит. Меньше времени уделяет домашним делам. К себе относится невнимательно, часто неопрятна, забывает умываться, чистить зубы, мыться, менять белье. На напоминания реагирует болезненно. Стала хуже готовить, часто еда, которую она приготовила, мало съедобна. Ест в комнате, иногда прямо из кастрюли, грязную посуду оставляет там же, запрещает убирать за собой, выбрасывает пищевые отходы тогда, когда они уже заплесневели и испортились. Не моет посуду, не убирает квартиру, считает, что в доме чисто и уборка не нужна. В последнее время имеют место и нарушения походки: стала ходить мелкими шажками, на широко расставленных ногах, испытывает сложности с поддержанием равновесия. Около месяца назад упала при выходе из магазина, около недели назад – при сходе с эскалатора. Оба раза падения происходили спонтанно, без каких-либо причин. В течение последнего месяца родственники пациентки отмечают, что она неопрятна мочой, пациентка это категорически отрицает. Ей бывает трудно заснуть, до глубокой ночи смотрит телевизор, комментирует происходящее, задает вопросы. Для лечения бессонницы, а также при эмоциональном перенапряжении после конфликтов с родственниками использует Валокордин или Корвалол (30–40 капель на прием). При этом она ходит в магазин, покупает продукты, трудностей при расчетах в магазине и получении пенсии не испытывает.
Около 20 лет назад у пациентки была выявлена артериальная гипертензия с эпизодическими подъемами артериального давления до 170–180 мм рт. ст. Своим «хорошим» давлением считает 110/70 мм рт. ст., поскольку «всегда была гипотоником». Осмотрена терапевтом, который назначил периндоприл 5 мг два раза в день и индапамид 1,5 мг с утра, однако препараты не применяет. В лечении артериальной гипертензии использует следующую схему: при «симптомах высокого давления», а именно тогда, когда ощущает тяжесть в голове или давящую головную боль в затылке, измеряет артериальное давление и, если оно более 130/70 мм рт. ст., принимает одну таблетку нифедипина под язык. Со слов пациентки, подобные «эпизоды повышения давления» возникают один-два раза в неделю.
Пациентка закончила среднеобразовательную школу и техникум. Работала бухгалтером, вышла на пенсию по возрасту. Курит по 10–20 сигарет в день с 30 лет. Бабушка и тетя пациентки страдали артериальной гипертензией, бабушка умерла в возрасте 72 лет от ишемического инсульта. Данных о перенесенных пациенткой инсультах нет, не госпитализировалась, не лечилась, не наблюдалась.
Соматический статус при осмотре. Артериальное давление – 160/95 мм рт. ст., частота сердечных сокращений – 80 в минуту, частота дыхания – 17 в минуту. Пациентка повышенного питания – 92 кг при росте 152 см.
Обследование. Электрокардиограмма: горизонтальное положение электрической оси сердца, диффузные изменения миокарда левого желудочка, мерцательная аритмия. Общий анализ крови без патологии. Биохимический анализ крови: холестерин – 7,0 ммоль/л, коэффициент атерогенности – 4,1, уровень сахара в крови – 4,6 ммоль/л. Дуплексное сканирование магистральных артерий головы: с двух сторон атеросклеротические бляшки в проекции бифуркации общей сонной и далее во внутренних сонных артериях, справа стеноз внутренней сонной артерии 45%, слева – 55%. Суточный мониторинг артериального давления: среднедневное систолическое артериальное давление – 142 мм рт. ст., диастолическое – 88 мм рт. ст., средненочное – 130/75 мм рт. ст. Максимальные значения артериального давления отмечаются утром с 10 до 12 часов (152/82 мм рт. ст.) и вечером с 18 до 21 часа (155/79 мм рт. ст.).
Неврологический статус. Пациентка ориентирована в месте, времени, собственной личности. Оживлен нижнечелюстной рефлекс, вызывается хоботковый рефлекс, рефлекс Маринеску – Радовичи с двух сторон. Сухожильные рефлексы живые, симметричные, парезов и патологических знаков нет. Чувствительных нарушений нет. Хватательный рефлекс с двух сторон, при просьбе не схватывать молоток пациентка может рефлекс подавить. Неустойчива, про-, ретро- и латеропульсии при проверке постурального ответа, не пытается удерживать равновесие. Походка осторожная, мелкими шажками, на широко расставленных ногах. Трудности прохождения поворотов, дверных проемов, инициации ходьбы (иногда делает один-два шага на месте перед тем, как начать движение, и при повороте).
Нейропсихологическое тестирование. Наблюдаются сложности при входе в задание, инертность, импульсивность, снижение внимания и скорости психических процессов. Быстро истощается, при длительных умственных нагрузках количество ошибок значительно возрастает, не видит их и не может исправить, теряет нить беседы, отвлекается, соскальзывает на другие темы разговора.
Настроение у пациентки хорошее, признаков тревоги и депрессии нет.
Нейровизуализационное исследование. Магнитно-резонансная томография: множественные лакуны в проекции базальных ганглиев, лобных долях, левом таламусе. Выраженный перивентрикулярный и субкортикальный лейкоареоз.
Таким образом, у пациентки с артериальной гипертензией, гиперхолестеринемией, ожирением, нарушениями ритма сердца, длительно курящей и не получающей лечения по поводу сердечно-сосудистой патологии, развились типичные СКР в сочетании с расстройствами поведения, постуральными и двигательными нарушениями. Указанные изменения носят флюктуирующий характер. Нарушение познавательных функций пациентки соответствует большому нейрокогнитивному расстройству (деменции).
Лечение сосудистых когнитивных расстройств
При ведении пациентов с СКР должны использоваться как медикаментозные (патогенетическая терапия, базовая симптоматическая терапия и неспецифическое лечение), так и немедикаментозные (когнитивный и моторный тренинг, психотерапия, когнитивная стимуляция) методы.
Медикаментозные методы
Лечение нужно начинать с патогенетической терапии – своевременного выявления и коррекции сердечно-сосудистой патологии, устранения сосудистых факторов риска. При обнаружении СКР пациент должен пройти детальное соматическое обследование с дальнейшей нормализацией артериального давления, уровней глюкозы и липидов в крови, коррекцией нарушений сердечного ритма и гиперкоагуляции. Если пациент курит, с ним нужно провести беседу о необходимости отказаться от табака. Исследования убедительно показывают, что адекватная коррекция сердечно-сосудистой патологии при СКР приводит к снижению риска развития и прогрессии когнитивных нарушений даже в отсутствие базовой симптоматической и метаболической терапии [6, 16, 23, 24]. Пациента необходимо проинформировать о важности изменения жизненного уклада: кроме отказа от курения, желательно изменить пищевые привычки и употреблять в пищу преимущественно овощи, фрукты, рыбу и мясо птицы, избегая животных жиров и мяса животных. При наличии избыточного веса следует позаботиться о нормализации массы тела, а кроме того, нарастить как физическую, так и умственную активность.
Препараты базисной симптоматической терапии отличаются от препаратов неспецифического лечения доказанной эффективностью в виде уменьшения выраженности когнитивных, поведенческих, эмоциональных нарушений, потребности в других лекарственных препаратах и времени госпитализации, улучшения качества жизни, замедлении скорости прогрессии когнитивных расстройств и так называемой фармакоэффективности (снижения прямых и непрямых расходов на лечение).
Базовая симптоматическая терапия включает два класса лекарственных препаратов: ингибиторы ацетилхолинэстеразы и антагонисты NMDA-рецепторов. В рандомизированных многоцентровых плацебоконтролируемых клинических исследованиях подтверждена эффективность ингибиторов ацетилхолинэстеразы при смешанной деменции. Изучение применения препаратов этой фармакотерапевтической группы у пациентов с сосудистой деменцией и недементными СКР было остановлено в связи с недоказанной эффективностью [6, 25, 26]. Таким образом, в базисной терапии СКР значительно чаще, чем ингибиторы ацетилхолинэстеразы, используются антагонисты NMDA-рецепторов, в частности мемантин (Акатинол Мемантин).
Как продемонстрировали проведенные исследования, Акатинол Мемантин эффективен и при большом нейрокогнитивном расстройстве (деменции), и при малом нейрокогнитивном расстройстве (умеренных когнитивных нарушениях) сосудистого генеза. Так, метаанализ доклинических исследований эффективности Акатинола Мемантина при болезни Альцгеймера, выполненный J. Folch и соавт., показал, что на фоне применения препарата повышается чувствительность к инсулину и предположительно уменьшается риск развития диабета второго типа, что в свою очередь снижает риск развития как болезни Альцгеймера, так и сосудистой деменции [27]. По данным недавно опубликованного исследования Y. Inoue и соавт., Акатинол Мемантин непосредственно способствует уменьшению отложений амилоида не только в веществе мозга (в том числе в структурах гиппокампового круга), но и в стенках сосудов [28]. Возможно, терапия препаратом Акатинол Мемантин положительно сказывается на состоянии пациентов с церебральной амилоидной ангиопатией и, как следствие, сокращает количество геморрагических инсультов при этой патологии.
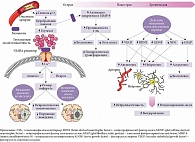
S. Seyedsaadat и D. Kalmes изучили результаты 19 доклинических исследований эффективности Акатинола Мемантина на моделях ишемии. Была подтверждена эффективность препарата в остром и острейшем периодах нарушения мозгового кровообращения (предположительно благодаря влиянию на зону ишемической полутени через систему глутамата и NMDA-рецепторов). Кроме того, продемонстрирована целесообразность применения препарата в реабилитации после перенесенного ОНМК. Так, Акатинол Мемантин сокращает срок реабилитации пациентов и улучшает ее качество, благоприятно воздействуя на нейро- и ангиогенез (рисунок) [29].
Выводы, полученные в результате метаанализа результатов экспериментальных исследований, были подтверждены M. Berthier и соавт., которые оценивали эффективность реабилитации пациентов с афазией (афазией Брока, Вернике, транскортикальной моторной и аномической, кондуктивной афазией) после перенесенного ишемического инсульта [30]. Нейропсихологическое состояние пациентов отслеживалось в динамике: им проводилось количественное нейропсихологическое тестирование до начала терапии, через 16 недель и далее каждые четыре недели. Все пациенты проходили речевую реабилитацию, а также случайным образом были распределены на получение препарата Акатинол Мемантин в дозе 20 мг в день (основная группа) или плацебо (контрольная группа). У пациентов основной группы восстановление речи происходило быстрее, статистические различия между группами отмечались с 16-й по 24-ю неделю исследования. Таким образом, включение Акатинола Мемантина в реабилитацию пациентов после перенесенного ОНМК может ускорить реабилитацию и улучшить ее качество.
И наконец, необходимо упомянуть результаты, полученные B. Jin и соавт., которые сравнивали эффективность и безопасность монотерапии ингибиторами ацетилхолинэстеразы (донепезилом, галантамином и ривастигмином) и мемантином (препарат Акатинол Мемантин) при СКР (всего 12 рандомизированных многоцентровых плацебоконтролируемых исследований) [31]. Оценивалось влияние терапии на когнитивные нарушения, поведение, повседневную активность и адаптацию. Отдельный анализ был проведен в отношении частоты встречаемости нежелательных явлений. На фоне терапии ривастигмином и донепезилом были получены положительные результаты в виде динамики общего балла краткой шкалы оценки психического статуса. Терапия донепезилом, галантамином и мемантином благоприятно сказывалась на когнитивных функциях (по когнитивной субшкале шкалы оценки нарушений при болезни Альцгеймера). Однако по шкале общего улучшения хорошие результаты продемонстрировал только мемантин. Кроме того, Акатинол Мемантин стал единственным препаратом, признанным более безопасным, чем плацебо. Частота нежелательных явлений на фоне терапии ривастигмином, донепезилом и галантамином значительно превосходила таковую и в группе плацебо, и в группе мемантина.
Немедикаментозные методы
Нелекарственные методы (когнитивно-моторный тренинг, когнитивная стимуляция, психотерапия) показаны всем пациентам с СКР как при умеренных, так и при выраженных нарушениях.
Эффективность сочетания когнитивного и моторного тренинга у пациентов с болезнью Альцгеймера и СКР доказана во многих исследованиях [6, 32–34]. Считается, что когнитивный тренинг может положительно влиять на уровень внимания и скорость психических процессов, что, несомненно, важно с учетом особенностей когнитивных нарушений при СКР. Вероятно, сочетание когнитивных нагрузок и достаточной двигательной активности улучшает состояние церебральной перфузии и метаболизма, а также чувствительность инсулиновых церебральных рецепторов к инсулину [33, 35]. Когнитивное стимулирование может иметь благоприятный эффект у пациентов с большим нейрокогнитивным расстройством, а психотерапия необходима при СКР, сочетающихся с эмоциональными и тревожными нарушениями.
Следует отметить, что единого подхода к методикам когнитивно-моторного тренинга у пациентов с когнитивными нарушениями различной степени выраженности нет. Группой авторов настоящей статьи разработаны методические рекомендации. Они учитывают особенности когнитивных нарушений при СКР, остром и острейшем периодах нарушений мозгового кровообращения, СКР и сердечно-сосудистой патологии на фоне перенесенных оперативных вмешательств. Методические рекомендации прошли успешную апробацию на базе клиники нервных болезней Первого МГМУ им. И.М. Сеченова и были внедрены в работу врачей-неврологов амбулаторного приема и стационара клиники. Более подробно о них будет рассказано в следующих статьях.
Заключение
В лечении СКР любой степени выраженности целесообразно использовать комплексный подход – сочетание лекарственных методов (патогенетическое лечение, базовая симптоматическая терапия и неспецифическая метаболическая терапия), а также нелекарственных методов лечения (когнитивно-моторного тренинга, когнитивной стимуляции, психотерапии). Комплексный подход дает лучший эффект в отношении как уменьшения выраженности существующих симптомов, так и дальнейшего развития заболевания.
A.A. Kindarova, S.A. Abdyshova, D. Fantalis, I.S. Preobrazhenskaya, PhD, Prof.
I.M. Sechenov First Moscow State Medical University
Contact person: Irina S. Preobrazhenskaya, irinasp2@yandex.ru
The article discusses the issues of etiology, pathogenesis, and features of drug and non-drug therapy of vascular cognitive disorders. Based on a clinical example, approaches to the diagnosis and treatment of cognitive disorders in patients with cardiovascular disease.