Ожирение: состояние проблемы и возможности терапии в XXI веке
- Аннотация
- Статья
- Ссылки
- English
В настоящее время установлено, что результатом сложного взаимодействия молекулярно-генетических, внутренних и внешних факторов является нарушение баланса между потреблением и расходом энергии, что приводит к накоплению жира. Жировой ткани отводится существенная роль в патогенезе ожирения. С особенностями ее отложения связан риск развития сопутствующих заболеваний и неблагоприятного прогноза. Кроме того, при всех формах ожирения нарушаются центральные механизмы регуляции поведенческих реакций.
Рассматриваются также вопросы дифференциальной диагностики и лечения ожирения.
В настоящее время установлено, что результатом сложного взаимодействия молекулярно-генетических, внутренних и внешних факторов является нарушение баланса между потреблением и расходом энергии, что приводит к накоплению жира. Жировой ткани отводится существенная роль в патогенезе ожирения. С особенностями ее отложения связан риск развития сопутствующих заболеваний и неблагоприятного прогноза. Кроме того, при всех формах ожирения нарушаются центральные механизмы регуляции поведенческих реакций.
Рассматриваются также вопросы дифференциальной диагностики и лечения ожирения.



Ожирение представляет одну из актуальных проблем XXI в. [1]. По оценкам экспертов Всемирной организации здравоохранения, в 2016 г. с избыточным весом насчитывалось 1,9 млрд лиц старше 18 лет, 650 млн из них страдали ожирением. Кроме того, увеличилась популяция детей старше пяти лет и подростков с ожирением – около 340 млн [2].
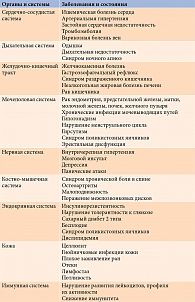
В настоящее время ожирение рассматривается не просто как избыточное накопление в организме жира, а как хроническое многофакторное рецидивирующее заболевание, ассоциированное с рядом серьезных кардиологических, метаболических, ревматологических, онкологических и других осложнений, нарушений психосоциального статуса (табл. 1) и приводящее к ранней утрате трудоспособности, а также преждевременной смерти [3, 4]. Так, если болезни сердечно-сосудистой системы занимают лидирующее место среди причин смертности в большинстве развитых стран, в том числе России, ожирение – среди потенциально устранимых причин летальных сердечно-сосудистых исходов [5]. Однако ожирение не всегда указывается в истории болезни.
Чаще всего встречается экзогенно-конституциональная форма ожирения, обусловленная систематическим перееданием и нерегулярной физической активностью, резким ограничением физической активности без коррекции привычного питания. Причиной развития ожирения также могут быть эндокринные и гипоталамические нарушения. Только в 2–3% случаев его удается связать с каким-либо заболеванием. Чаще это заболевания эндокринной системы.
Среди факторов риска развития ожирения указывают наследственную предрасположенность и генетическую обусловленность, однако определяющим является образ жизни. Речь, в частности, идет о таких особенностях современного образа жизни, как переедание, высококалорийное питание, преобладание в рационе жиров (насыщенных жиров, трансжиров), простых углеводов, снижение двигательной активности, курение, злоупотребление алкоголем, а также ряд социальных и поведенческих факторов [6].
На риск развития ожирения оказывают влияние и перинатальные факторы (излишний набор веса матерью в период гестации, нутритивный статус матери, низкая или большая масса тела при рождении) [2, 7].
Результатом сложного взаимодействия молекулярно-генетических, внутренних и внешних факторов является нарушение баланса между потреблением и расходом энергии. Энергетический расход организма складывается из трех частей [6]: основного обмена, специфического динамического действия пищи (термогенез) и физической активности. На основной обмен расходуется 60–65% энергии, термогенез – 10%, физическую нагрузку – 20–40%. У женщин скорость основного обмена на 10% ниже, чем у мужчин, так как меньше масса и поверхность тела. Суточная внутри- и межиндивидуальная вариабельность составляет от 2,0 до 10,0 и от 7,5 до 18,0% соответственно [8]. С возрастом скорость основного обмена снижается. Исследования с участием близнецов свидетельствуют, что генетический фактор определяет примерно 40% основного обмена [9].
На сегодняшний день продолжительный положительный энергетический баланс, который возникает при потреблении пищи в количестве, превышающем расход энергии, либо снижении расхода энергии, считается одним из основных механизмов развития ожирения [6].
Патогенетические механизмы
В патогенезе ожирения и ассоциированных с ним заболеваний существенная роль отводится жировой ткани (ЖТ), которая признана самостоятельным секреторным органом. Жировая ткань выполняет ауто-, пара- и эндокринную функции [6]. Она секретирует большое количество цитокинов с разными биологическими эффектами. В частности, они способны вызывать сопутствующие избыточному накоплению массы тела нарушения, в том числе развитие инсулинорезистентности (ИР). По мере развития ожирения не только увеличиваются размер и количество адипоцитов, но и изменяется их функциональная активность. Как следствие, нарушается баланс адипоцитокинов, регулирующих чувствительность рецепторов к инсулину [10].
Топографическими особенностями отложения ЖТ в значительной степени определяется риск развития сопутствующих ожирению заболеваний и неблагоприятного прогноза.
В настоящее время выделяют висцеральную (интраабдоминальную), расположенную вокруг внутренних органов жировую ткань (ВЖТ), и подкожную жировую ткань. Под ВЖТ понимают общее количество интраабдоминального жира, включая интраперитонеальный (мезентериальный и сальниковый), который дренируется в портальную систему. Висцеральный жир при нормальном весе в среднем составляет от 6 до 20% общей массы тела (табл. 2). Меньшая часть ВЖТ находится в забрюшинном пространстве [11].
Примерно 85% жировой ткани располагается в подкожно-жировой клетчатке [12].
В отличие от подкожной жировой ткани ВЖТ лучше иннервирована, содержит большее количество адипоцитов на единицу массы ткани, более широкую сеть капилляров, обильную иннервацию и непосредственно сообщается с портальной системой. Кроме того, экспрессия многих цитокинов более выражена именно в адипоцитах висцеральной жировой ткани, которая играет ключевую роль в развитии и прогрессировании ИР и ее проявлений [13, 14]. Накопление макрофагов также происходит преимущественно в висцеральной жировой ткани [15].
Увеличение количества висцеральных адипоцитов приводит к изменению конформации молекулы инсулинового рецептора и нарушению связывания его с инсулином [10]. Кроме того, адипоциты висцерального жира в отличие от адипоцитов подкожного жира характеризуются высокой плотностью и чувствительностью бета-адренорецепторов (особенно третьего типа), рецепторов кортизола, андрогенов, но низкой плотностью и чувствительностью альфа-адренорецепторов и рецепторов инсулина [14].
Описанные выше метаболические признаки жировых клеток определяют повышенную чувствительность висцеральных адипоцитов к липолитическим воздействиям и, наоборот, низкую – к антилиполитическому эффекту инсулина [16].
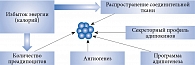
Поскольку ЖТ может изменять свой размер, особый интерес представляет концепция ограниченной ее способности к увеличению как фактора, сопрягающего ожирение с ИР [17]. Считается, что жировая ткань имеет пределы по максимальному увеличению собственной массы. На определенном этапе у конкретного индивидуума объем жировой ткани достигает максимальных значений, после чего уже не может увеличиваться. В результате жир накапливается в органах. Факторы, которые могут влиять на способность жировой ткани к увеличению объема, многочисленны. Среди них и генетические факторы, и средовые (рис. 1) [18].
Итак, на фоне накопления липидов в адипоцитах и увеличения их размеров нарушается способность последних аккумулировать триглицериды. Это приводит к отложению жира в разных органах и тканях (скелетных мышцах, печени, сердце и периваскулярно, поджелудочной железе) и их дисфункции, а также дальнейшему нарастанию системной ИР [18].
При всех формах ожирения нарушаются центральные механизмы регуляции поведенческих реакций. Ключевыми регуляторами потребления пищи и энергетического баланса признаны латеральная и вентромедиальная области гипоталамуса. Первая регулирует чувство голода, вторая контролирует чувство насыщения. Нарушение любого звена этого сложного механизма может привести к изменениям потребления пищи и депонированию жира [19].
Одни моноамины и пептиды – нейропептид Y, галанин, опиоиды, соматолиберин, грелин, бета-эндорфин, соматостатин обладают орексигенными эффектами и увеличивают потребление пищи, другие – норадреналин, серотонин, кортиколиберин, тиролиберин, холецистокинин, меланоцитостимулирующий гормон, лептин характеризуются анорексигенными свойствами и, напротив, снижают потребление пищи [6].
Немаловажное значение в развитии ожирения имеет эндоканнабиноидная система (ЭКС). Это нейрорегуляторная эндогенная сигнальная система, отвечающая за многие метаболические процессы, включая энергетический гомеостаз, липидный и углеводный обмен, термогенез, потребление пищи и расход энергии, пищевое поведение [20, 21]. ЭКС также участвует в процессах запоминания, формирования эмоций и чувства боли. Употребление вкусной, высококалорийной и насыщенной жирами пищи приводит к гиперактивации ЭКС, увеличению аппетита и усилению липогенеза [22]. ЭКС включает каннабиноидные рецепторы 1 и 2 типов (CB1 и CB2) – G-белковые рецепторы, их эндогенные лиганды, белки, участвующие в их синтезе, транспорте и метаболизме, а также внутриклеточные сигнальные пути [23, 24]. Рецепторы CB1 экспрессируются преимущественно в центральной нервной системе (особенно в гиппокампе, коре головного мозга, мозжечке и базальных ганглиях), а также в жировой ткани, костной системе, желудочно-кишечном тракте, эндокринных органах, рецепторы CB2 – в иммунных и гемопоэтических клетках (Т-клетках, В-клетках и моноцитах) [24].
В экспериментальных работах показано, что активация СВ1-рецепторов под влиянием фито- и эндоканнабиноидов стимулирует прием пищи даже у сытых животных. При этом мыши, нокаутированные по рецептору СВ1, резистентны к алиментарному ожирению – по сравнению с контролем съедают гораздо меньше после периода депривации еды. У грызунов также отмечено повышение активности симпатической нервной системы, термогенеза и усиление окисления жиров. Селективная блокада CB1-рецепторов уменьшает потребление пищи и массу тела [25].
Результаты исследований на животных и клинических испытаний свидетельствуют, что блокада рецепторов CB1 способствует снижению массы тела, кардиометаболических факторов риска и ИР [22, 24–26].
Получены данные, что каннабиноидные рецепторы ответственны за трансформацию клеток белой жировой ткани в бежевые или коричневые адипоциты, поэтому модуляцию их активности можно считать потенциальной мишенью при ожирении. Установлено также, что, воздействуя на термогенную функцию белой и коричневой жировой ткани, агонисты и блокаторы CB1-рецепторов могут влиять на массу тела посредством ингибирования и стимуляции расхода энергии, что, несомненно, имеет клиническое значение [27].
Таким образом, современные исследования доказали, что накопление жира сопровождается усилением активности ЭКС, увеличением экспрессии CB1-рецепторов и концентрации эндоканнабиноидов в плазме и жировой ткани (анандамида и 2-арахидоноил-глицерола), особенно при абдоминальном ожирении.
Методы оценки
Основным критерием ожирения является чрезмерное накопление жировой ткани в организме. Наиболее адекватный показатель содержания жира в организме – индекс массы тела (ИМТ). Он рассчитывается по формуле: масса тела : рост². Согласно определению Всемирной организации здравоохранения, ожирение диагностируется при ИМТ ≥ 30 кг/м². ИМТ от 30,0 до 34,9 кг/м² соответствует ожирению первой степени, от 35,0 до 39,9 кг/м² – второй степени, более 40 кг/м² – ожирению третьей степени (морбидному ожирению). При ИМТ от 25 до 29,9 кг/м² говорят об избыточной массе тела.
При одинаковом ИМТ абдоминальное ожирение ассоциируется с более высоким риском развития сердечно-сосудистых заболеваний, сахарного диабета 2 типа, чем периферическое (гиноидное) ожирение. В клинической практике окружность талии (ОТ) используется как суррогатный маркер увеличения абдоминального жира, поскольку коррелирует с количеством ВЖТ. Данный показатель также связан с риском кардиометаболических заболеваний [28]. ОТ и ИМТ в равной степени отражают общее количество жировой ткани в организме, однако именно ОТ позволяет получить информацию о характере распределения жира в организме, в большей степени о ВЖТ. Так, о висцеральном ожирении у мужчин свидетельствует увеличение ОТ более 94 см, у женщин – более 80 см [29]. Абдоминальное ожирение четко связано с ИР и метаболическими нарушениями.
Дифференциальная диагностика
Следует помнить, что ожирение может быть одним из клинических проявлений других заболеваний. В дифференциально-диагностическом плане органические причины ожирения имеют место не более чем у 1% больных. В большинстве случаев такие причины ожирения, как гиперкортицизм, гипотиреоз, гипогонадизм, церебральные формы патологии, возможно исключить при сборе анамнеза и осмотре пациента. В то же время не стоит забывать, что ожирение способно влиять на функцию эндокринных желез.
Установить причину увеличения массы тела и провести дифференциальную диагностику различных форм ожирения позволяют дополнительные методы обследования.
В большинстве случаев гиперкортицизм может быть исключен уже при осмотре пациента. Ожирение, прогрессирующая прибавка массы тела с типичным перераспределением подкожно-жировой клетчатки с преимущественным отложением жира в области шеи, груди, живота, на лице (лунообразное лицо) при тонких конечностях вследствие атрофии мышечной ткани указывает на синдром гиперкортицизма. Последний приводит к выраженному истончению кожи с появлением типичных багрово-красных стрий до 1 см. Их следует дифференцировать с бледно-розовыми тонкими полосами растяжения, возникающими при быстром наборе массы тела у больных ожирением. Исключить гиперкортицизм возможно с помощью ночного подавляющего теста с 1 мг дексаметазона, оценки уровня кортизола в слюне или суточной экскреции кортизола с мочой.
Снижение основного обмена, термогенеза, задержка жидкости могут способствовать небольшой прибавке массы тела у пациентов с гипотиреозом. В тех случаях, когда причиной ожирения является гипотиреоз, избыток массы тела обычно незначительный, аппетит снижен. Для гипотиреоза характерны заторможенность, адинамичность больного, понижение температуры тела, брадикардия, тестоватые отеки и другие признаки дефицита тиреоидных гормонов. При этом потливость отсутствует. У таких пациентов должна быть оценена функция щитовидной железы (определен уровень тиреотропного гормона). Следует помнить о возможности сочетания экзогенно-конституционального ожирения и гипотиреоза. При таком варианте заместительная терапия L-Тироксином не приведет к снижению массы тела.
При расстройстве либидо для исключения гиперпролактинемического гипогонадизма и гипотиреоза необходимо определить уровень тестостерона, пролактина, тиреотропного гормона. Увеличение массы тела при синдроме гиперпролактинемии обусловлено повышением уровня пролактина, в результате чего увеличивается синтез жиров из углеводов, а также снижением уровня эстрогенов у женщин, тестостерона у мужчин. Характерные симптомы синдрома гиперпролактинемии у женщин – галакторея, нарушение менструального цикла, бесплодие. Клиническим подтверждением гиперпролактинемии у мужчин являются гинекомастия, симптомы гипогонадизма, снижение либидо. Кроме того, пациентов часто беспокоят головные боли. После подтверждения стойкого повышения уровня пролактина необходимо провести магнитно-резонансную томографию головного мозга с контрастным усилением.
При редкой форме вторичного ожирения на фоне гипоталамо-гипофизарных заболеваний жировая ткань откладывается преимущественно в области груди, ягодиц, бедер, нижней части живота. Наблюдаются отставание в росте и развитии, недоразвитие половых органов (малый размер половых органов, отсутствие менструации, либидо и половой потенции). У мужчин отсутствуют волосы на лобке и под мышками. При обследовании отмечаются признаки повышения внутричерепного давления, связанного с опухолевым процессом: головные боли, изменение полей зрения, увеличение размеров турецкого седла.
Цель и методы лечения
Ожирение представляет собой междисциплинарную проблему, поэтому лечить таких пациентов должны врачи разных специальностей. Установлено, что только при своевременном вмешательстве заболевание обратимо.
Склонность к рецидивам требует пожизненного врачебного контроля и в большей степени самоконтроля потребления пищи и состояния здоровья.
Цель лечения – снижение массы тела до уровня, при котором максимально уменьшается риск для здоровья, улучшается течение и прогноз заболеваний, ассоциированных с ожирением, а также долгосрочное поддержание достигнутого результата.
Для улучшения состояния здоровья не обязательно стремиться к достижению идеальной массы тела: клинически значимое снижение массы тела составляет не менее 5–10% от исходной. Это выполнимо для большинства больных. У пациентов с ИМТ > 35 кг/м2 целью терапии является снижение массы тела на 10% от исходной величины.
Согласно последним европейским рекомендациям, управление ожирением направлено на предотвращение развития осложнений, сопутствующих заболеваний (или адекватное лечение в случае, если они уже есть), поддержку метаболического здоровья (по возможности), борьбу против стигматизации и восстановление положительного восприятия своего тела, самооценки, хорошего самочувствия [29]. При выборе цели лечения по снижению массы тела в долгосрочной перспективе необходимо учитывать наличие ассоциированных с ожирением заболеваний и состояний (метаболический синдром, сахарный диабет 2 типа, дислипидемия, артериальная гипертензия, неалкогольная жировая болезнь печени, синдром поликистозных яичников, ночное апноэ). Ожидаемое снижение массы тела составляет от 5 до 15% в зависимости от сопутствующей патологии (табл. 3).
Очень важна скорость снижения массы тела. Резкое похудение может ухудшить течение коморбидной патологии, в частности часто встречающейся при ожирении неалкогольной жировой болезни печени из-за ускоренной мобилизации жира из депо и отложения его в печени. Оптимальным считается постепенное умеренное снижение массы тела – от 0,5 до 1,0 кг/нед в первые три – шесть месяцев или на 5,0% за три месяца (при наличии сахарного диабета 2 типа – на 3,0%) с последующей его стабилизацией в течение полугода [29].
После достижения эффекта необходимо предпринимать меры по поддержанию достигнутых результатов и предупреждению рецидивов заболевания.
Немедикаментозная терапия
Первой линией терапии ожирения является изменение образа жизни (рациональное питание, повышение физической активности, поведенческая терапия) (табл. 4).
Основой немедикаментозного вмешательства считается рациональное низкокалорийное питание, ограничение жиров (особенно насыщенных) и легкоусвояемых углеводов в течение длительного периода времени. Похудение и отрицательный энергетический баланс достигаются снижением физиологической калорийности рациона на 500–600 ккал/сут, что приводит к снижению массы тела в среднем на 0,5 кг/нед. Однако суточная калорийность пищи не должна быть менее 1200 ккал у женщин и менее 1500 ккал у мужчин. Минимальная энергетическая потребность у пациентов с нормальным весом, находящихся на постельном режиме, составляет приблизительно 1150 ккал/сут (0,8 ккал/мин).
К основным принципам рационального питания относятся:
- регулярный прием пищи, наличие полноценного завтрака, ограничение перекусов;
- медленный прием пищи (чувство сытости появляется примерно через 20 минут от начала еды);
- постепенное уменьшение объема порций;
- употребление в пищу продуктов, содержащих клетчатку, с низким гликемическим индексом;
- исключение продуктов, стимулирующих аппетит (острые, пряные, копченые и соленые закуски, алкогольные напитки).
Продукты без ограничения употребления должны создавать ощущение насыщения (рыба, птица, нежирные сорта мяса), наполненности желудка (овощи, лиственная зелень). При составлении рациона особое внимание обращают на метаболические нарушения. При дислипидемии требуется ограничить поступление с продуктами питания холестерина – до 250–300 мг/сут. В случае артериальной гипертензии – снизить потребление соли до 5 г/сут.
Физическая активность играет важную роль в снижении массы тела и поддержании достигнутого результата при соблюдении главного условия – регулярности. Важно подчеркнуть, что при похудении без физических нагрузок пациент с ожирением, как правило, теряет не только жировую, но и мышечную массу. Сохранить последнюю позволяют физические нагрузки. Регулярная физическая активность уменьшает количество висцерального жира и кардиометаболические риски. Согласно результатам исследований, для мобилизации висцерального жира достаточно 300 мин/нед умеренной или 150 мин/нед интенсивной двигательной активности [29]. Больным могут быть рекомендованы регулярные аэробные нагрузки малой и средней интенсивности: дозированная ходьба со скоростью 5–6 км/ч, плавание, занятия на тренажерах. В начале терапии пациенты часто не могут переносить продолжительные и интенсивные занятия. Однако в дальнейшем объем и интенсивность физической активности должны наращиваться.
Контроль снижения массы тела предусматривает ежедневное ведение дневника питания, в котором указываются все приемы пищи, полный перечень продуктов и их объем, количество потребленной жидкости.
Несмотря на серьезность проблемы, терапевтический эффект немедикаментозных методов нередко неудовлетворительный, большинство пациентов худеют очень медленно, занимают пассивную позицию. Так, среди пациентов, снизивших массу тела на фоне немедикаментозных вмешательств, около двух третей вновь набирают потерянный вес в течение года, а большинство – в последующие пять лет. В некоторых случаях масса тела становится больше исходной.
Фармакотерапия
Медикаментозные методы лечения используют в качестве дополнения к немедикаментозным. Они позволяют не только повысить приверженность пациентов лечению, но и более эффективно снизить массу тела, а также удержать достигнутый результат в течение длительного времени.
Препараты для лечения ожирения назначают при ИМТ ≥ 30,0 или от 27,0 до 29,9 кг/м² при наличии ассоциированных с ожирением заболеваний (табл. 4). Если за три месяца немедикаментозных вмешательств масса тела не снижается на 5%, при наличии сахарного диабета – на 3%, также необходимо назначить фармакотерапию [29].
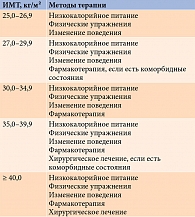
В последних европейских рекомендациях по лечению ожирения у взрослых указано, что методы терапии зависят и от ИМТ, и ОТ (табл. 5) [29].
В России для лечения ожирения зарегистрировано несколько лекарственных средств.
Фармакологическое действие сибутрамина (препарат центрального действия, применяется один раз в день в дозе 10–15 мг) обусловлено селективным торможением обратного захвата серотонина и норадреналина из синаптической щели нейронов центральной нервной системы, регулирующих пищевое поведение. Воздействуя на обе стороны энергетического обмена, сибутрамин способствует снижению массы тела. Данный препарат противопоказан при неконтролируемой артериальной гипертензии (артериальное давление ≥ 145/90 мм рт. ст.), ишемической болезни сердца, нарушении сердечного ритма, сердечной недостаточности, эпилепсии, печеночной и почечной недостаточности, глаукоме, терапии ингибиторами моноаминоксидазы и антидепрессантами. От приема сибутрамина следует воздержаться во время беременности и лактации [30].
Орлистат – единственный препарат периферического действия, не обладающий системными эффектами. Его действие направлено на основную причину ожирения – усвоение жирной пищи. Назначается по 120 мг три раза в день во время или непосредственно после приема пищи. Ингибируя липазы желудочно-кишечного тракта, орлистат препятствует расщеплению и последующему всасыванию пищевых жиров – до 30%. За счет этого создается хронический дефицит энергии, что при длительном приеме способствует снижению массы тела. Противопоказаниями к применению орлистата являются синдром мальабсорбции, холестаз, гиперчувствительность к препарату или его компонентам [31].
Лираглутид – аналог человеческого глюкагоноподобного пептида 1. Препарат произведен с помощью биотехнологий. Лираглутид вводят подкожно один раз в день. Начальная доза составляет 0,6 мг/сут, затем ее увеличивают до 3 мг/сут с шагом 0,6 мг и интервалами не менее одной недели для улучшения переносимости со стороны желудочно-кишечного тракта. Активируя рецепторы глюкагоноподобного пептида 1, лираглутид действует как анорексигенный гормон (снижает аппетит, объем потребляемой пищи). Лираглутид регулирует аппетит с помощью усиления чувства наполненности желудка и насыщения, одновременно ослабляя чувство голода и уменьшая предполагаемое потребление пищи. Противопоказаниями для применения являются медуллярный рак щитовидной железы в анамнезе, в том числе семейном, множественная эндокринная неоплазия второго типа, тяжелая депрессия, суицидальные мысли или поведение, в том числе в анамнезе, нарушение функции почек и печени тяжелой степени, сердечная недостаточность третьего и четвертого функционального класса (в соответствии с классификацией NYHA) [32].
Как уже отмечалось ранее, хроническая гиперактивность ЭКС вносит существенный вклад в патогенез ожирения [20–23]. В 2010 г. в Российской Федерации зарегистрировано референтное лекарственное средство для лечения ожирения ‒ препарат Диетресса, разработанный ООО «Научно-производственная фирма „Материа Медика Холдинг“». Активными компонентами данного препарата являются технологически обработанные аффинно очищенные антитела (сверхвысокие разведения) к каннабиноидному рецептору 1 (анти-CB1). Через механизмы аллостерической модуляции препарат сенситизирует CB1-рецепторы, что сопровождается повышением их чувствительности к эндогенным каннабиноидным нейропептидам. Вследствие этого нормализуется эндоканнабиноидная регуляция мезолимбической системы, в том числе пищевого центра в гипоталамусе.
Центральные эффекты Диетрессы сочетаются с периферическими ‒ влиянием на СВ1-рецепторы адипоцитов, следствием чего является активация основного обмена.
Применение препарата приводит к уменьшению потребления пищи и массы тела без тормозящего либо стимулирующего влияния на центральную нервную систему у лиц с избыточной массой тела и ожирением первой и второй степени [33].
Эффективность препарата Диетресса доказана в двух двойных слепых плацебоконтролируемых рандомизированных клинических исследованиях [22]. Первое, с участием 146 амбулаторных пациентов старше 18 лет с избыточной массой тела и ожирением, проводилось в десяти ведущих клинических центрах России. В рамках исследования оценивали изменение выраженности чувства голода, а также долю пациентов с избыточной массой тела и ожирением первой и второй степени, у которых масса тела снизилась на 5% и более через три месяца терапии. В ходе исследования отмечено значимое различие эффективности терапии данным препаратом и плацебо у пациентов с первой степенью ожирения – 2,9 против 3,3 балла соответственно. Выраженность чувства голода среди пациентов, получавших препарат Диетресса, уменьшалась уже в первый месяц терапии и сохранялась в последующий период наблюдения [22].
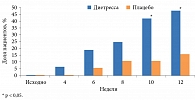
Среди пациентов с ожирением первой степени, принимавших Диетрессу, через десять недель лечения был 41% похудевших, через 12 недель – 47%, что достоверно отличалось от количества таких пациентов в группе плацебо – 10 и 15% соответственно (p < 0,05 в каждом из указанных случаев) (рис. 2).
Второе плацебоконтролируемое исследование разных схем применения Диетрессы (по одной таблетке шесть раз или по две таблетки три раза в день) с участием 493 пациентов с ожирением также продемонстрировало значимое снижение массы тела в течение шести месяцев терапии у пациентов с ожирением первой степени. Обе схемы применения препарата были сопоставимы по эффективности [34]. Динамика средних ежемесячных потерь веса на фоне двух схем лечения значимо превосходила изменение веса в группах плацебо – 49 (первая схема) и 48% (вторая схема) против 33 и 21% (p < 0,05 в каждом из указанных случаев).
Принимая во внимание тот факт, что лечение пациентов с ожирением требует комплексного подхода, в том числе с применением психотерапевтических методик, позволяющих изменить поведенческие стереотипы, было проведено экспериментально-психологическое исследование, включавшее 98 пациентов с избыточной массой тела и ожирением первой степени [35]. Пациенты участвовали в программе формирования нового стиля жизни и питания по методике Help people change, 51 из них в дополнение к психологической коррекции получал препарат Диетресса по шесть таблеток в день в течение трех месяцев. Оценка параметров психологического статуса проводилась с помощью анкетирования.
На фоне терапии препаратом Диетресса наблюдалось изменение пищевого поведения. По окончании первого месяца для 74% пациентов еда перестала быть основным источником удовольствия. Помимо снижения аппетита через две-три недели приема препарата чувство насыщения возникало при употреблении небольшой порции некалорийной пищи. У 72% пациентов в следующие шесть – восемь месяцев после отмены препарата сохранялся достигнутый эффект без рикошетного повышения аппетита и прибавки массы тела.
Модуляция функциональной активности ЭКС под влиянием препарата Диетресса (за счет воздействия как на центральные, так и на периферические СВ1-рецепторы) регулирует энергетический и субстратный обмен и, что немаловажно, пищевое поведение. Это способствует снижению массы тела у пациентов с ожирением [22].
Важно отметить, что после похудения необходимо осуществлять меры по поддержанию достигнутых результатов и предупреждению рецидивов заболевания. Снижение скорости метаболизма с развитием синдрома низкого трийодтиронина затрудняет дальнейшую потерю массы тела у многих пациентов. Препарат Диетресса также можно назначать для поддерживающей терапии в период стабилизации массы тела, когда снижается скорость основного обмена.
E.V. Biryukova, MD, PhD, Prof., N.M. Platonova, MD, PhD
A.I. Yevdokimov Moscow State University of Medicine and Dentistry
National Medical Research Center for Endocrinology
Contact person: Elena V. Biryukova, lena@obsudim.ru
Discussed the urgency of obesity problem and its pathogenesis. Now it is established that the result of the complex interaction of molecular-genetic, internal and external factors is the violation of the balance between energy’s expenditure and consumption, which leads to the fat accumulation. Adipose tissue plays the significant role in the pathogenesis of obesity. The risk of concomitant diseases development and unfavorable prognosis is associated with the peculiarities of its deposition. In addition, in the case of all forms of obesity the central mechanisms of behavioral reactions regulation are being violated.
As well, the article discusses the differential diagnosis and treatment of obesity.
