Тактика ведения пациентов с язвенным колитом, не ответивших на лечение анти-ФНО
- Аннотация
- Статья
- Ссылки
- English
Представлено клиническое наблюдение пациентки с язвенным колитом, не ответившей на лечение препаратом анти-ФНО. Отражены современные подходы к диагностике язвенного колита и тактике лечения, а также терапевтические возможности по преодолению вторичной неэффективности ингибиторов ФНО с помощью применения ингибиторов янус-киназ.
Представлено клиническое наблюдение пациентки с язвенным колитом, не ответившей на лечение препаратом анти-ФНО. Отражены современные подходы к диагностике язвенного колита и тактике лечения, а также терапевтические возможности по преодолению вторичной неэффективности ингибиторов ФНО с помощью применения ингибиторов янус-киназ.


Язвенный колит (ЯК) – хроническое заболевание толстой кишки, характеризующееся иммунным воспалением ее слизистой оболочки [1].
Как и болезнь Крона, ЯК является современной проблемой гастроэнтерологии. Это связано в первую очередь с отсутствием точной этиологии, существованием нескольких теорий развития заболевания, отсутствием однозначных критериев диагностики. Факторы, способствующие формированию воспалительного процесса в слизистой оболочке толстой кишки, многочисленны: генетическая предрасположенность, иммунные нарушения, сбои в функционировании кишечной микрофлоры [2], кишечная проницаемость, состояние гомеостаза и протективных свойств слизистой оболочки толстой кишки [3].
Согласно зарубежным данным, заболеваемость ЯК составляет от 0,6 до 24,3 на 100 тыс. человек, распространенность достигает 505 на 100 тыс. человек. Данные о распространенности ЯК в Российской Федерации ограничены. Распространенность ЯК выше в северных широтах и в западных регионах. Заболеваемость и распространенность ЯК в Азии ниже, однако в настоящее время наблюдается тенденция к их увеличению. Европеоиды страдают заболеванием чаще, чем представители негроидной и монголоидной рас. Первый пик заболеваемости отмечается между 20 и 30 годами жизни, второй – в возрасте 60–70 лет с приблизительно одинаковой частотой у мужчин и женщин [1].
Для клинической картины ЯК характерны [2]:
- хроническая диарея длительностью более шести недель (дифференциальный диагноз с инфекционной диареей);
- примесь слизи (у 50% больных) или крови (40%) в стуле;
- боль в животе (у 70% больных);
- частая продолжительная боль в правой подвздошной области;
- необъяснимая анемия;
- интоксикация;
- необъяснимая лихорадка;
- снижение массы тела (у 60% больных).
К наиболее частым внекишечным проявлениям, которые встречаются у 5–20% пациентов с ЯК, относят поражение суставов (моно- и полиартриты крупных суставов, артралгии, артропатии мелких суставов, сакроилеит), поражение кожи (узловатая эритема, гангренозная пиодермия), поражение глаз (увеит, иридоциклит, эписклерит). При наличии внекишечных проявлений необходима консультация специалистов: врача-ревматолога, врача-дерматовенеролога, врача-офтальмолога; а при наличии беременности обязательна консультация врача акушера-гинеколога [4].
Золотой стандарт диагностики ЯК отсутствует, диагноз устанавливается на основании сочетания данных анамнеза, анализа клинических симптомов заболевания, данных толстокишечной эндоскопии и гистологического исследования. Кроме указанных исследований, согласно Клиническим рекомендациям по диагностике и лечению язвенного колита от 2020 г. МЗ РФ [1], рекомендованы следующие обследования: магнитно-резонансная томография органов брюшной полости, компьютерная томография (КТ) органов брюшной полости с контрастированием кишечника, ультразвуковое исследование (УЗИ) органов брюшной полости, ирригоскопия с двойным контрастированием. В последние годы в клинической практике широко используются ультразвуковые методы исследования: трансабдоминальное ультразвуковое исследование толстой кишки, трансабдоминальное ультразвуковое исследование прямой кишки и анального канала. Дополнительными методами исследования при наличии показаний могут быть видеокапсульная эндоскопия, одно- или двухбаллонная энтероскопия [1]. Кроме вышеуказанных обязательных методов диагностики, в настоящее время широко используются и неинвазивные лабораторные методы, в частности определение фекального кальпротектина, который играет вспомогательную роль в выявлении заболевания и применяется с целью динамического наблюдения за течением ЯК и как метод контроля за эффективностью лечения.
Лечебная тактика при ЯК включает в себя назначение лекарственных препаратов, диетические ограничения, психосоциальную поддержку.
Основными целями лечения являются:
- быстрое купирование острых атак ЯК;
- достижение и поддержание бесстероидной ремиссии (прекращение приема глюкокортикостероидов (ГК) в течение 12 недель после начала терапии);
- предупреждение и устранение осложнений;
- своевременное назначение хирургического лечения при отсутствии терапевтического эффекта от проводимого лечения или при прогрессировании процесса, а также при развитии опасных для жизни пациента осложнений.
При составлении плана лечения ЯК необходимо учитывать:
- протяженность поражения толстой кишки;
- тяжесть текущей атаки;
- наличие внекишечных проявлений;
- наличие гормональной зависимости или резистентности;
- наличие и характер осложнений.
Лекарственные препараты, назначаемые пациентам с ЯК, условно подразделяют на несколько групп:
- средства для индукции ремиссии: 5-аминосалициловая кислота (месалазин), системные ГК (преднизолон и метилпреднизолон), топические ГК (будесонид), иммуносупрессоры (азатиоприн, 6-меркаптопурин, метотрексат), антибиотики, биологические генно-инженерные лекарственные средства – моноклональные антитела к фактору некроза опухоли альфа (ФНО-α) (инфликсимаб, адалимумаб, цертолизумаба пэгол, голимумаб) и моноклональные антитела к интегрину альфа-4-бета-7 (ведолизумаб), действующие селективно только в желудочно-кишечном тракте. С 2018 г., кроме таргетных биологических препаратов, для индукции ремиссии при среднетяжелом и тяжелом ЯК также применяется таргетный синтетический препарат – ингибитор янус-киназ (тофацитиниб) [1];
- средства для поддержания ремиссии (противорецидивные средства): 5-аминосалициловая кислота, иммуносупрессоры, биологические генно-инженерные лекарственные средства или ингибитор янус-киназ [1];
- вспомогательные лекарственные средства: препараты железа для коррекции анемии, препараты для инфузионной терапии с целью коррекции белково-электролитных нарушений, средства для профилактики остеопороза (препараты кальция) и др. [2].
При воспалительных заболеваниях кишечника (ВЗК) к базисным препаратам относятся препараты 5-аминосалициловой кислоты и иммуносупрессоры. Базисные препараты, применяемые для лечения ВЗК, оказывают противовоспалительное и иммуносупрессивное действие, но они могут ингибировать как патологические, так и защитные реакции организма. В настоящее время доказано, что основой развития воспаления при ВЗК является дисбаланс между противовоспалительными и провоспалительными цитокинами. При этом ключевую роль отводят ФНО-α [5, 6].
К препаратам, которые являются антителами к этому провоспалительному цитокину, относятся инфликсимаб, адалимумаб, голимумаб, цертолизумаба пэгол. В настоящее время для лечения среднетяжелых и тяжелых атак ЯК применяется ведолизумаб – гуманизированное моноклональное антитело, которое связывается с интегрин-альфа-4-бета-7 – белком клеточной мембраны, ответственным за миграцию лейкоцитов в слизистую оболочку кишечника. Включение в клиническую практику биологических препаратов, безусловно, приводит к улучшению лечения умеренного и тяжелого ЯК, однако от 10 до 20% пациентов утрачивают ответ в течение года, что приводит к необходимости оптимизации дозы или перехода на другой препарат [7].
Это послужило мощным стимулом к изучению новых подходов к фармакотерапии ЯК.
В течение последнего десятилетия была разработана новая группа селективных иммуносупрессоров, применяемых при различных аутоиммунных заболеваниях. Они представляют собой низкомолекулярные химически синтезированные препараты, ингибирующие внутриклеточные сигнальные молекулы янус-киназы (JAK). Углубление знаний об иммунопатогенезе иммуновоспалительных заболеваний (ИМЗ) и роли JAK в регуляции иммунного ответа и воспаления стимулировало разработку новых ингибиторов JAK и расширение показаний для их назначения при ревматических и неревматических ИМЗ. Иммуномодулирующие и противовоспалительные свойства ингибиторов JAK на молекулярном уровне связаны с одновременной модуляцией эффектов широкого спектра важных провоспалительных цитокинов, а не только отдельных цитокинов, что характерно для большинства генно-инженерных биологических препаратов.
Первым ингибитором янус-киназ является тофацитиниб, который был одобрен для лечения ревматоидного артрита в 2012 г. Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (США), а в 2017 г. – Европейским агентством по лекарственным средствам. С 2018 г. показания для тофацитиниба были расширены: он также зарегистрирован для назначения при псориатическом артрите и ЯК в РФ, ЕС, США и других странах мира. Тофацитиниб (Яквинус) в первую очередь ингибирует JAK3 и JAK1 и в меньшей степени – JAK2 и TYK2. Он избирательно и обратимо связывается с участком связывания аденозинтрифосфата в янус-киназе. Этот механизм блокирует передачу сигнала от рецепторов клеток к их ядру для многих важных интерлейкинов (IL-2, IL-4, IL-6, IL-7, IL-15 и IL-21) и интерферонов I и II типов, тем самым модулируя воспалительные и иммунные реакции [8, 9]. Несмотря на то что препарат принимается внутрь, клинический ответ регистрируется уже в течение первой недели применения. Выраженная клиническая эффективность обычно наблюдается через 2–8 недель после начала лечения.
Клиническое наблюдение
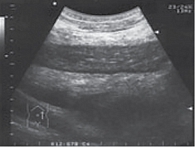
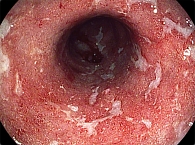
Пациентка К., 50 лет, инвалид третьей группы. Впервые обратилась за медицинской помощью в кабинет ВЗК Областного гастроэнтерологического центра (ОГЭЦ) БУЗ ВО «Воронежская областная клиническая больница № 1» в августе 2015 г. с жалобами на жидкий стул до шести раз в сутки со слизью и прожилками крови, боли в средних и нижних отделах живота в основном в ночное время, в связи с чем у пациентки нарушился сон и, как следствие, наблюдалась слабость, снижение работоспособности. Из анамнеза: за последние шесть месяцев за пределы РФ не выезжала, антибиотики и нестероидные противовоспалительные препараты не принимала, вредных привычек не имеет, семейный анамнез не отягощен. Пациентка осмотрена гастроэнтерологом и колопроктологом. При объективном осмотре: состояние удовлетворительное. Кожные покровы чистые, тургор удовлетворительный. Питания удовлетворительного (рост 164 см, вес 65 кг). Костно-мышечная система без особенностей. Периферические лимфоузлы не увеличены. Со стороны органов кровообращения и органов дыхания патологии не выявлено. Осмотр органов пищеварения: язык влажный, слегка обложен белым налетом. Живот правильной формы, участвует в дыхании, аускультативно – перистальтика удовлетворительная, при пальпации отмечалась болезненность по ходу толстой кишки. Печень, селезенка не увеличены. Пациентке назначено общеклиническое, биохимическое, ультразвуковое и эндоскопическое исследования согласно Клиническим рекомендациям по диагностике и лечению язвенного колита [1]. В результате исследования было выявлено увеличение скорости оседания эритроцитов (СОЭ) – 22 мм/ч, уровня С-реактивного белка – 12,4 мг/л, фекального кальпротектина – 120 мкг/г. Ультразвуковое исследование толстой кишки: слепая кишка, восходящая ободочная, поперечно-ободочная кишка – стенка утолщена до 2 мм, структура сохранена, прослеживается, гаустрация сохранена. Нисходящая ободочная кишка: стенка утолщена до 3 мм, структура сохранена, прослеживается, гаустрация сглажена, высота гаустр – до 1 мм. Сигмовидная кишка: стенка утолщена до 3,5 мм, структура сохранена, прослеживается, гаустрация сглажена, высота гаустр – до 1 мм. Заключение: УЗ-признаки диффузных изменений стенки нисходящей ободочной и сигмовидной кишки воспалительного генеза (рис. 1). Толстокишечная эндоскопия: выраженный колит, вероятно ЯК. Сфинктерит. Патолого-гистологическое заключение: хронический неспецифический высоактивный эрозивный колит-проктит, без признаков опухолевого роста. В результате проведенного комплексного обследования, консультаций гастроэнтеролога и колопроктолога был поставлен диагноз: язвенный колит, впервые выявленный, левостороннее поражение, активность по Truelоve и Witts 1–2 (рис. 2).
Пациентка была госпитализирована в гастроэнтерологическое отделение. Назначена комбинированная базисная терапия: месалазин (Салофальк) 3 г/сут и пена (Салофальк) 2 г/сут. Через две недели состояние пациентки улучшилось: уменьшилась частота стула до двух раз в сутки без примесей слизи и крови; снизились показатели уровня С-реактивного белка до 7,8 мг/л, фекального кальпротектина до 76 мкг/г, СОЭ до 17 мм/ч. Пациентка выписана из стационара для продолжения лечения в амбулаторных условиях. Было рекомендовано продолжить прием комбинированной терапии в течение восьми недель с последующей консультацией в кабинете ВЗК Областного гастроэнтерологического центра для оценки результатов лечения. Однако в указанные сроки пациентка на прием не явилась.
В июне 2016 г. самочувствие пациентки ухудшилось: частота стула увеличилась до 10 раз в сутки, в кале появились слизь и прожилки крови, боли в животе, боли в суставах. Пациентка обратилась за медицинской помощью в ОГЭЦ. Было выяснено, что пациентка отметила улучшение самочувствия после восьминедельного курса лечения и далее самостоятельно прекратила прием препаратов. В связи с наличием рецидива ЯК пациентка была госпитализирована в гастроэнтерологическое отделение для проведения комплексного обследования. В лабораторных исследованиях было выявлено: лейкоцитоз – 12,52 × 10-9/л; анемия – уровень гемоглобина 96 г/л; увеличение СОЭ – 48 мм/ч, С-реактивного белка – 32,4 мг/л, фекального кальпротектина – до 243 мкг/г. Результаты ультразвукового, эндоскопического и патоморфологического исследований подтвердили наличие ЯК: левостороннее поражение, среднетяжелое течение. Пациентке назначено лечение: преднизолон 60 мг/сут, антибактериальная терапия, азатиоприн 100 мг/сут, месалазин 3 г/сут, пена Салофальк 2 г/сут. Через 10 дней отмечена положительная динамика: уменьшились клинические проявления, улучшились лабораторные показатели: число лейкоцитов в пределах нормальных значений, уровень гемоглобина – 115 г/л, СОЭ – 24 мм/ч, С-реактивный белок – 12,2 мг/л, фекальный кальпротектин – 105 мкг/г. Пациентка выписана для продолжения лечения в амбулаторных условиях, был предложен график посещения гастроэнтеролога и колопроктолога кабинета ВЗК ОГЭЦ. Но в связи с несоблюдением графика посещения специалистов ОГЭЦ пациенткой, а также самостоятельной отменой преднизолона через два месяца симптомы заболевания рецидивировали. При ухудшении состояния пациентка принимала преднизолон разово. В связи с нестабильным течением ЯК, которое проявлялось частыми рецидивами в виде увеличения частоты стула, повышением температуры, неинтенсивными болями в животе и суставах, пациентке потребовалась неоднократная (август 2017 г.; ноябрь 2017 г.; июль 2018 г.) госпитализация в гастроэнтерологическое отделение Воронежской областной клинической больницы № 1. В 2019 г. в связи с неэффективностью проводимой терапии пациентка была направлена в Национальный медицинский исследовательский центр (НМИЦ) колопроктологии им. А.Н. Рыжих, где находилась на стационарном лечении с 08.04.2019 по 26.04.2019. По результатам колоноскопии от 12.04.2019: эндоскопическая картина ЯК, тотальная форма, минимальная активность в сигмовидной и прямой кишке. УЗИ от 10.04.2019: УЗ-признаки ЯК, левостороннее поражение, незначительная активность воспалительного процесса в сигмовидной и прямой кишке. Пневматизированная, расширенная в правых отделах ободочная кишка. Диффузные изменения паренхимы печени. Деформация желчного пузыря. УЗ-признаки хронического панкреатита. Миома матки. Кистозно измененный левый яичник. УЗ-признаки спаечного процесса в полости малого таза. КТ-энтерография от 24.04.2019: КТ-картина более характерна для ЯК, левостороннее поражение, с активностью процесса в прямой кишке. Киста левого яичника. В связи с наличием гормональной зависимости пациентке по жизненным показаниям было рекомендовано проведение биологической терапии препаратом голимумаб (Симпони). В НМИЦ колопроктологии им. А.Н. Рыжих проведен курс индукционной терапии. Рекомендована поддерживающая терапия по месту жительства: введение каждые четыре недели по 50 мг п/к. По окончании индукционного курса состояние пациентки улучшилось, лабораторные показатели воспаления – в пределах нормальных значений. В октябре 2019 г. на фоне проводимой терапии препаратом голимумаб (Симпони) (после шести введений) состояние пациентки снова ухудшилось: увеличилась частота стула до 15 раз с кровью, отмечалось повышение температуры и боли в суставах. Пациентка госпитализирована в гастроэнтерологическое отделение Воронежской областной клинической больницы № 1. Обострение ЯК сопровождалось повышением уровня лейкоцитов (11,1 × 10-9/л), увеличением СОЭ – 25 мм/ч, повышением уровня С-реактивного белка до 76 ед/л, фекального кальпротектина – до 345 мкг/г. Назначена терапия: преднизолон в дозе 60 мг/сут, антибактериальная терапия, азатиоприн 100 мг/сут. На фоне проводимой терапии состояние пациентки улучшилось, рекомендовано продолжить прием преднизолона, азатиоприна и введение препарата голимумаб. После окончания терапии преднизолоном у пациентки вновь наблюдался рецидив заболевания, который проявлялся в увеличении частоты стула до шести‑семи раз в сутки с кровью, болью в животе, ложными позывами. Пациентка повторно была направлена в НМИЦ колопроктологии им. А.Н. Рыжих, где находилась на лечении с 12.02.2020 по 18.02.2020. При выписке рекомендовано продолжить терапию препаратом голимумаб (Симпони). Продолжение лечения не обеспечило ремиссии: частота стула пять-шесть раз в сутки с примесью слизи и крови, ложные позывы к дефекации четыре‑пять раз в сутки, снижение веса за 1,5 месяца на 4 кг, боли в суставах. Проведено эндоскопическое исследование толстой кишки: сигмовидная кишка – слизистая гиперемирована, отечная, с налетом фибрина, контактно легко ранима. Сосудистый рисунок отсутствует. Подобная эндоскопическая картина прослеживалась и в прямой кишке. Морфологическое исследование слизистой прямой и сигмовидной кишки: кусочки слизистой толстой кишки с изъязвлением, грануляциями, деформированными криптами, эпителий с укрупненными ядрами, интраэпителиальными нейтрофилами, крипт-абсцессы, в строме диффузная лимфоплазмоцитарная инфильтрация с примесью эозинофилов, нейтрофилов, полиповидный кусочек с удлиненными, деформированными криптами. Заключение: морфологическая картина соответствует ЯК высокой активности, с изъязвлением, псевдополипом,
грануляциями.
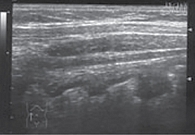
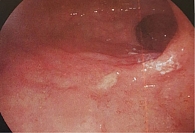
В связи с отсутствием ремиссии ЯК в октябре 2020 г. проведена консультация в системе видеоконференцсвязи со специалистами НМИЦ колопроктологии. С учетом неоднократных рецидивов ЯК рекомендован перевод пациентки на терапию таргетным синтетическим препаратом тофацитиниб (Яквинус). В декабре 2020 г. пациентке начат индукционный курс тофацитинибом: 20 мг/сут в течение восьми недель. Переносимость индукционного курса новым препаратом была хорошей. Через две недели от начала терапии тофацитинибом состояние улучшилось: уменьшилась частота стула до четырех раз в сутки без слизи и крови, отсутствовали ложные позывы, значительно уменьшилась частота и интенсивность болей в животе. По окончании индукционного курса пациентка жалоб не предъявляла: частота стула один‑два раза в сутки без слизи и крови, отсутствовали тенезмы и боли, пациентка прибавила в весе. Контрольное УЗИ: нормальная стенка толстой кишки, без признаков воспаления (рис. 3). Результаты контрольной колоноскопии показали отсутствие признаков воспаления (рис. 4).
Пациентка продолжила прием тофацитиниба (Яквинуса) в дозе 10 мг/сут. В течение последующих четырех месяцев состояние пациентки расценивалось как стабильно удовлетворительное.
Пациентка постоянно находилась под наблюдением гастроэнтеролога областного гастроэнтерологического центра Воронежской областной клинической больницы № 1. Проводили мониторинг течения ЯК (динамика основных клинических проявлений), данных лабораторных показателей активности патологического процесса в толстой кишке (табл. 2).
Заключение
Применение препарата нового класса селективных иммуносупрессоров – ингибиторов янус-киназ является высокоэффективным новым подходом к лечению иммуноопосредованных воспалительных заболеваний, в том числе и ЯК. Тофацитиниб (Яквинус) обладает быстрым фармакологическим действием при пероральном применении. Представленный клинический пример продемонстрировал высокую эффективность тофацитиниба в индукционной и поддерживающей терапии пациентки с ЯК, не ответившей на лечение базисными и генно-инженерным препаратами. Лечение тофацитинибом (Яквинусом) характеризовалось хорошей переносимостью.
V.I. Mordasova, D.V. Kopylova, PhD, G.V. Dobrosotskih
Voronezh Regional Clinical Hospital № 1
Contact person: Valentina I. Mordasova, mordasova1976@inbox.ru
Effective methods of treating UC patients is one of the most important problems. The inclusion of biological drugs in clinical practice leads to an improvement in the treatment of moderate and severe UC, but from 10 to 20% of patients lose their response within a year, which leads to the need to optimize the dose or switch to another drug. The use of janus kinase inhibitors – a new class of targeted synthetic drugs for the treatment of active ulcerative colitis – allows for a rapid clinical response when switching from TNF-α inhibitors. Pronounced clinical efficacy is usually observed 2-8 weeks after the start of treatment.
A clinical case of a patient with ulcerative colitis who did not respond to treatment with anti-TNF is presented. Modern approaches to the diagnosis of ulcerative colitis and treatment tactics are reflected, as well as therapeutic possibilities for overcoming the secondary inefficiency of TNF inhibitors by using janus kinase inhibitors.

