Наследственные дистрофии сетчатки – не приговор! Инновации в мир света и красок. XVI Российский общенациональный офтальмологический форум
- Аннотация
- Статья
- Ссылки
В России насчитывается более 1300 пациентов с установленным диагнозом НДС. Однако статистика заболеваемости может быть выше, поскольку постановка окончательного диагноза в клинической практике может занимать несколько лет. Раннее распознавание патологии и обследование сокращают время установления диагноза и начала лечения. Об этом, а также о методах диагностики, инновационных методах генной терапии и маршрутизации пациентов рассказали участники XVI Российского общенационального офтальмологического форума (РООФ)2.
В России насчитывается более 1300 пациентов с установленным диагнозом НДС. Однако статистика заболеваемости может быть выше, поскольку постановка окончательного диагноза в клинической практике может занимать несколько лет. Раннее распознавание патологии и обследование сокращают время установления диагноза и начала лечения. Об этом, а также о методах диагностики, инновационных методах генной терапии и маршрутизации пациентов рассказали участники XVI Российского общенационального офтальмологического форума (РООФ)2.
Успехи и потенциал генной терапии
Генная терапия – метод лечения или профилактики с помощью доставки генетического материала в организм пациента. Разработанная в 1970-х гг. концепция данного вида терапии доказала возможность переноса генетической информации. Было также сделано предположение, что при адаптации генома человека станет возможной коррекция наследственных заболеваний с помощью правильной копии гена, заменяющей мутировавшую.
Как отметил Павел Игоревич Макаревич, к.м.н., заведующий лабораторией генно-клеточной терапии Института регенеративной медицины Университетской клиники Московского государственного университета им. М.В. Ломоносова, человеческий геном содержит полную «библиотеку чертежей» всех белков нашего организма. Генная терапия относится к изменению его белковой части, которая составляет 1,5–2% всего генома3.
Поломка или системные сбои в кодирующих белки генах способны приводить к развитию наследственных заболеваний. В данном случае генная терапия – единственный вид этиотропной терапии, то есть лечения причины, а не последствий, вызванных мутацией (например, ферментозамещающая терапия).
За последние 20 лет помимо генной терапии онкологических заболеваний появилось множество наследственных моногенных заболеваний, для которых либо разработан, либо находится в процессе разработки этот тип лечения. Офтальмология – не исключение. Таким образом, это направление заняло очень весомое место среди таких заболеваний благодаря более чем 4000 проведенных изысканий в данной области. Результатом исследований стала разработка высокоэффективных препаратов4.
Генная терапия заключается как во введении вирусного или невирусного вектора в организм человека, так и в выделении клеток из той или иной ткани и создании здоровой копии гена в отдельном сосуде вне организма человека. Для переноса генетической информации как внутри организма человека, так и вне используются природные механизмы – векторы. В генной терапии применяются невирусные и вирусные векторы.
Вектор – носитель, осуществляющий доставку нуклеиновых кислот в клетки. На текущий момент в терапии используются вирусные (аденовирусы, ретровирусы, лентивирусы, вирус простого герпеса человека, бакуловирусы), невирусные векторы (плазмидная ДНК, незащищенная РНК), вспомогательные молекулы и комплексы (липосомы, белковые комплексы, липидные комплексы, органические полимеры), а также вспомогательные методы (механические, физические и химические)5, 6.
Генная терапия применяется и при НДС. В настоящее время в мире проводится свыше 35 клинических исследований7.
Поскольку внедрение генетической информации возможно в большое количество тканей организма, имеются перспективы применения генной терапии и при патологиях в переднем сегменте глаза8.
Вирусная генная терапия в отличие от невирусной пока может применяться однократно, поскольку далее вырабатывается иммунитет. Исследований, подтверждающих возможность повторного применения такой терапии, недостаточно.
Зарегистрированный препарат воретиген непарвовек представляет собой вектор, несущий ДНК с нормальным геном RPE65. С помощью субретинальной инъекции он вводится в глазное яблоко, после чего происходят трансдукция и экспрессия нормального гена RPE65. Дегенерация останавливается9–11.
По словам эксперта, генная терапия не может заставить заново сформироваться те структуры, которые уже погибли. Сказанное относится ко многим подобным дегенеративным заболеваниям. После необратимой стадии поражения терапия неэффективна.
Орфанные показания могут нести как преимущества, так и недостатки для генной терапии. Среди преимуществ – целесообразность, возможность излечения заболевания, особый регуляторный статус12. К недостаткам можно отнести высокую стоимость терапии из-за очень маленького объема выборки, применение терапии только в раннем возрасте, недоверие пациентов и отсутствие релевантной животной модели для оценки эффективности. В действительности при использовании любого препарата должен соблюдаться баланс эффективности, доступности, этичности и безопасности.
Роль врача амбулаторного звена в диагностике наследственной дистрофии сетчатки
Наследственные дистрофии сетчатки – обширная группа генетически гетерогенных заболеваний заднего сегмента глаза13. Эти заболевания включены в перечень орфанных (распространенность не более 1 на 10 тыс. населения).
Идентифицировано свыше 250 генов, являющихся причинным фактором развития НДС14. Существует несколько типов наследования НДС:
- аутосомно-доминантный;
- аутосомно-рецессивный;
- Х-сцепленный.
Основными заболеваниями, которые можно отнести к НДС, считаются пигментный ретинит, болезнь Штаргардта, вителлиформные макулодистрофии (бестрофинопатии, включая болезнь Беста), цилиопатии (синдромы Ашера и Барде – Бидля), врожденный амавроз Лебера, колбочковая и колбочко-палочковая дистрофии1. Патогенез таких заболеваний, как правило, идентичен: прогрессирующая потеря функций фоторецепторов со снижением зрения вплоть до слепоты1.
Осуществляя ведение пациентов с синдромальной НДС, врач должен обращать внимание на внеглазные проявления и уточнять у родителей в случае синдрома Барде – Бидля, есть ли у ребенка такие симптомы, как нанизм, ожирение, полидактилия, гипогонадизм, поликистоз почек, а в случае синдрома Альстрема опрашивать родителей на предмет наличия у ребенка в прошлом ожирения, пигментного ретинита, сенсоневральной тугоухости, кардиопатии и нефропатии.
Особое внимание следует уделить орфанным заболеваниям, поддающимся этиотропному лечению. Речь идет об аутосомно-рецессивном изолированном пигментном ретините 20-го типа и врожденном амаврозе Лебера 2-го типа, вызванными биаллельными мутациями гена RPE65 и поэтому схожими между собой, однако отличающимися возрастом манифестации заболевания.
Пигментный ретинит чаще возникает у детей от трех лет и старше, в большей степени у подростков. Среди жалоб – никталопия, сужение полей зрения, потеря периферического поля зрения, снижение темновой адаптации. В целях диагностики врач проверяет зрение, цветовое зрение, уточняет информацию о том, как ребенок видит вечером и в сумерках (видит ли ребенок звезды). Для данного заболевания характерна триада симптомов11, 15: пигментация сетчатки в виде «костных телец», восковидная бледность диска зрительного нерва, уменьшение количества сосудов, изменение калибра артериол (истончение). Оптическая когерентная томография (ОКТ) позволяет обнаруживать истончение наружных сегментов с уменьшением толщины наружного ядерного слоя или полную их потерю. Золотым стандартом в диагностике и оценке прогрессирования пигментного ретинита остается электроретинография16–18.
Врожденный амавроз Лебера проявляется в младенчестве и на первых месяцах жизни. Зачастую родители сами приходят к врачу первичного звена с жалобами, например, на то, что ребенок не фиксирует взгляд, не следит за игрушкой, болезненно реагирует на свет (или, наоборот, пристально смотрит на свет), трет глаза и давит на них. При этом заболевании характерны минимальные изменения на глазном дне. В случае прогрессирования патологического процесса изменения структур глазного дна (хориоретинальная дегенерация, перифовеальная атрофия, «костные тельца», пигментация, субретинальные пятна, «мраморное» глазное дно, пигментные изменения на уровне пигментного эпителия сетчатки, бледность диска зрительного нерва) развиваются изолированно или в сочетании друг с другом11, 18.
Зачастую пациенты немногословны, поэтому задача врача – подробно расспросить пациента или его близкого, задать уточняющие вопросы и поставить цель – заподозрить наследственную дистрофию сетчатки.
Основные методы обследования2 для установления правильного диагноза включают в себя:
- клинико-инструментальные (комплексное офтальмологическое обследование: визометрия, диагностика нарушения цветового зрения, прямая офтальмоскопия с использованием щелевой лампы и высокодиоптрийных линз, оптическая когерентная томография заднего сегмента глаза, поля зрения по Гольдману или статическая компьютерная периметрия; электрофизиологическое исследование: электроретинография (ЭРГ) (смешанная, или палочко-колбочковый ответ; высокочастотная ритмическая ЭРГ на 30 Гц фликер, а также зрительные вызванные потенциалы – на вспышку и реверсивный паттерн));
- молекулярно-генетические (этап I: анализ ДНК методом высокопроизводительного секвенирования кастомной панели Ophthalmo, включающей кодирующие последовательности таргетных генов; этап II: семейный сегрегационный анализ методом прямого секвенирования по Сэнгеру).
Алгоритм офтальмологического осмотра ребенка, у которого заподозрена НДС, следующий2:
- визометрия – определение остроты зрения;
- офтальмоскопия с мидриазом:
- характеристика пигментного эпителия (наличие и степень выраженности признаков атрофии – область, мкм);
- характеристики макулы (наличие и степень атрофии);
- характеристики диска зрительного нерва;
- участок сетчатки размером ≥ 3 дисковых участков сетчатки без атрофии или пигментной дегенерации в пределах заднего полюса (да/нет);
- компьютерная периметрия:
- поля зрения (степени для конкретных стимулов III4e, V4e);
- остальные поля зрения в пределах 30 градусов фиксации, измеренные изоптером III4e или эквивалентом (да/нет);
- электороретинограмма: латентность и амплитуда;
- ОКТ.
Дополнительно могут быть проведены следующие исследования11:
- аутофлуоресценция – гипер-, гипо-, нормофлюоресценция;
- электроокулография (%, коэффициент Ардена);
- OКT-ангио (индекс плотности сосудов, площадь неперфузии, мм2, индекс кровотока – единицы (среднее (SD), медиана, мин., макс.), зрительно вызванные потенциалы: латентность, мс, амплитуда, мВ, порог световой чувствительности зрительного поля (log10 (кд∙с/м2)).
По словам Марины Сергеевны ПЕТРАЧКОВОЙ, и.о. руководителя клинико-диагностического центра Национального медицинского исследовательского центра здоровья детей, с.н.с., врача-офтальмолога, к.м.н., очень важно, чтобы врачи знали, что есть НДС, для которых предусмотрено этиотропное лечение. Необходимо своевременно выявлять таких пациентов и в полном объеме оказывать им медицинскую помощь.
У врачей-офтальмологов остаются и нерешенные вопросы. Например, отсутствуют утвержденные клинические рекомендации и стандарты оказания медицинской помощи при постановке диагноза НДС, четкий алгоритм ведения пациентов с НДС, а также не всегда есть четкое понимание причинно-следственной связи патогенеза и клинического проявления НДС.
Для повышения осведомленности врачей об НДС, расширения знаний об этих заболеваниях, помощи врачам в определении и постановке диагноза создан образовательный сайт «Поиск света», где подробно описаны НДС, симптомы, диагностика, а также представлена карта центров диагностики НДС в каждом регионе. Специалисты по НДС могут оставить на этом сайте свои контакты и будут рады ответить на вопросы врачей по этой теме.
Офтальмогенетика и инновации в терапии НДС
Начиная разговор об инновациях НДС, следует прежде всего определиться с терминологией. Понятие «офтальмогенетика» не выделено в отдельную дисциплину, но очевидно, что это междисциплинарный клинический раздел, неразрывно связанный с медицинской генетикой и офтальмологией и с разных сторон изучающий этиологию, патогенез, диагностику, лечение, реабилитацию и абилитацию с учетом генетического предиктора и изменений генетического аппарата, приводящих к изменению органов зрения. Подробнее стоит остановиться на ключевых для данной темы определениях.
Офтальмогенетика – научно-клинический раздел медицины на стыке генетики и офтальмологии, направленный на изучение эпидемиологии, этиологии, патогенеза, течения и лечения наследственных глазных болезней (наследственной офтальмопатологии).
Наследственная офтальмопатология – группа заболеваний глазного яблока и/или придаточного аппарата органа зрения, как изолированных, так и входящих в симптомокомплекс синдромной патологии, этиологическим фактором развития которого является измененный генетический материал, повлекший за собой изменение конечного белкового продукта, участвующего в формировании одной или нескольких структур органа зрения.
Сегодня в России в полном объеме реализован так называемый полный цикл офтальмогенетики, в который входят такие разделы, как наука, клиника, образование и лечение. В аспекте науки основная задача – показать научному и клиническому сообществу актуальность проблемы наследственной офтальмопатологии.
Несмотря на то что НДС считаются орфанными заболеваниями, статистика показывает, что реальная распространенность наследственной офтальмопатологии – 1 на 1715 офтальмологических пациентов. 35% всех пациентов, обращающихся к офтальмологам, имеют генетический предиктор, о чем важно помнить для корректной диагностики и постановки диагноза. Можно выделить эндемические зоны. Например, распространенность наследственных патологий сетчатки среди малых этнических народов (ногайцы, карачаевцы, осетины и др.) в два раза выше.
Актуальным остается и вопрос классификации19 наследственных заболеваний с поражением органов зрения. Самым удобным подходом считается классификация по топографическому признаку. Наследственная патология сетчатки является лидирующей на данный момент – около 37% всех наследственных заболеваний органов зрения. При этом изменения генетического аппарата могут быть абсолютно разными, как моногенными, так и хромосомными, и все они приводят к патологии заднего сегмента. Не стоит забывать и о мутации митохондриальной ДНК. Эта проблема также требует консультации генетика.
Согласно данным, полученным лабораторией генетической эпидемиологии Медико-генетического центра (МГНЦ) им. академика Н.П. Бочкова за 17 лет исследований в области офтальмогенетики в России, наиболее часто встречаются такие патологии, как макулярная дистрофия сетчатки глаза или болезнь Штаргардта, пигментный ретинит и амавроз Лебера.
Следует обратить внимание и на генетическую гетерогенность (случаи, когда за заболевание отвечают мутации в разных генах) и клинического полиморфизма НДС. Среди российских пациентов наиболее распространенной формой амавроза Лебера является 2-й тип, хотя в зарубежной литературе частота таких случаев – около 5%.
Виталий Викторович КАДЫШЕВ, руководитель научно-клинического центра генетики глазных болезней, заведующий кафедрой офтальмогенетики Института ВиДПО МГНЦ им. академика Н.П. Бочкова, ведущий научный сотрудник лаборатории генетической эпидемиологии, куратор по наследственным глазным болезням РФ, врач-генетик, офтальмолог высшей квалификационной категории МГНЦ им. академика Н.П. Бочкова, к.м.н., профессор РАЕ, отметил, что не следует забывать о колбочковых, палочко-колбочковых и колбочко-палочковых дистрофиях. Ведь они достаточно часто мимикрируют под себя, и истинного амавроза Лебера не наблюдается. Во входящих диагнозах регулярно фигурирует диагноз «палочко-колбочковая дистрофия». И это правильно, потому что амавроз Лебера в первую очередь поражение фоторецепторного аппарата. Конечно, врач, диагностировавший палочко-колбочковую дистрофию, заслуживает уважения, особенно если он еще и направил пациента на консультацию к врачу-генетику. Фактически такую консультацию следует проводить 100% пациентов, особенно детского возраста.
Как уже отмечалось, существует несколько типов наследования НДС – аутосомно-доминантный, аутосомно-рецессивный и Х-сцепленный. Гены были изучены в соответствии с формами заболеваний, и определены мажорные гены, часто встречающиеся в популяции российских пациентов:
- десять мажорных генов (80,5%) для аутосомно-рецессивных форм изолированной наследственной офтальмопатологии сетчатки (ABCA4, CNGB3, RPE65, GUCY2D, CNGA3, DNAJC30, EYS, CEP290, NR2E3, USH2A);
- девять генов (67,9%) для аутосомно-доминантных форм (BEST1, OPA1, RHO, CRB1, SNRP200, PRPF31, PRPF8, PITPNM3, ABCA4);
- три гена (78,8%) для Х-сцепленных рецессивных форм (RS1, RPGR, GPR143).
Диагностика таких заболеваний также требует междисциплинарного подхода. Что касается клинико-инструментальных методов, отдельного внимания заслуживают молекулярно-генетические, расшифровкой и интерпретацией которых должен заниматься только врач-генетик. Эти методы включают в себя:
- секвенирование NGS;
- прямое секвенирование по Сэнгеру;
- мультиплексную лигазозависимую амплификацию (MLPA);
- флуоресцентную гибридизацию in situ (FISH-метод);
- функциональный анализ/протогеномное исследование;
- масс-спектрометрию.
Первые два имеют первостепенное значение.
В настоящее время в России врачам и пациентам доступен ряд программ для ДНК-диагностики – бюджетные (региональные и федеральные) и специальные целевые программы.
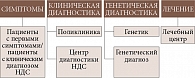
В МГНЦ им. академика Н.П. Бочкова был разработан комплексный алгоритм междисциплинарной диагностики НДС, где четко определены этапы диагностики на каждом уровне медицинской организации, от амбулаторного звена до стационара, и алгоритм действий в случае, когда пациент доходит до уровня медико-генетической консультации у врача-генетика или в медико-генетическом центре (рисунок). Этот алгоритм также показывает, как будет строиться ДНК-диагностика и какие пациенты будут направлены на генную терапию в специализированные офтальмологические центры.
Несмотря на то что существует и алгоритм маршрутизации пациента, клиническая диагностика занимает в среднем два-три года до того момента, когда пациента направят на консультацию к генетику.
Почти на каждом уровне такой диагностики встречаются сложности. На уровне симптомов имеется недостаточная информированность пациентов о возможностях ДНК-диагностики и таргетной терапии. Уровень клинической диагностики характеризуется сосредоточенностью пациента на приеме офтальмолога первичного звена, слабой информированностью врачей первичного звена о профилях пациентов с НДС, что подчеркивает важность тщательного сбора анамнеза при осмотре пациентов офтальмологами, недостаточностью оснащения оборудованием и навыков работы на специализированном оборудовании (при его наличии). На уровне генетической диагностики отсутствуют парадигмы маршрутизации пациентов к генетикам для верификации диагноза, что связано и с организационными проблемами, и с недоступностью помощи в ряде регионов20.
Какова же практическая значимость офтальмогенетики и всех проведенных исследований? За рубежом проводятся 54 исследования в рамках разработки новых молекул. Однако в клиническую практику на данный момент внедрен только один генный препарат. В России же за последние четыре года было выявлено 40 таргетных взрослых пациентов и детей, из них пролечено 20 детей за счет средств фонда «Круг добра» единственным зарегистрированным в России в 2022 г. препаратом воретиген непарвовек21.
Важно отметить, что в России полностью отработано междисциплинарное взаимодействие профильных учреждений, функционирует междисциплинарный научно-клинический центр генетики глазных болезней в МГНЦ им. академика Н.П. Бочкова. Клинические рекомендации по НДС, разработанные совместно со специалистами Национального медицинского исследовательского центра глазных болезней им. Гельмгольца и ряда других специализированных учреждений, сейчас находятся на рассмотрении.
Заключение
Прошедший конгресс РООФ и сателлитный симпозиум «Наследственные дистрофии сетчатки – не приговор! Инновации в мир света и красок» продемонстрировали важность обучения и повышения уровня знаний врачей в области офтальмогенетики, в частности НДС, для того, чтобы использовать окно возможностей, своевременно устанавливать верный диагноз и назначать лечение, направленное на улучшение качества жизни и сохранение зрения. Для повышения квалификации специалистов существует ряд возможностей, например курсы кафедры офтальмогенетики Института высшего и дополнительного профессионального образования МГНЦ, а также сайт «Поиск света», на котором размещается информация об НДС, симптомах, методах диагностики и лечения, а также карта центров диагностики, где пациенты и врачи могут получить консультацию и помощь.
736038/C&GMed/DIG/10.23/1