Стресс, тревога и когнитивные расстройства
- Аннотация
- Статья
- Ссылки
- English
От физиологического стрессового ответа к патологической тревоге: три ключевые теории развития расстройств тревожного спектра
Чтобы понять, какими путями тревога приводит к расстройствам когнитивной сферы, нужно вспомнить ключевые патофизиологические механизмы развития расстройств тревожного спектра.
Для патологической тревоги характерно нарушение формирования адекватной связи «опасность – страх», когда наблюдается несоответствие между степенью реальной угрозы и физиологическим ответом организма [1]. В норме в ответ на сигнал опасности активируется миндалина (ключевой центр страха), которая посредством афферентов получает информацию из соответствующих ассоциативных корковых центров [2]. Благодаря исходящим проводящим путям к центрам вегетативной нервной системы – гипоталамусу, островковой доле и другим структурам миндалина запускает базовую стрессовую реакцию по принципу «драться или убегать». В результате активируются сердечно-сосудистая система, различные катаболические процессы, иммунные реакции, что обеспечивает готовность к максимально быстрому физическому ответу, который позволит либо противостоять возникшей опасности, либо в случае неравности угрозе спастись бегством [3].
У животных подобная физиологическая реакция вполне обоснованна: возникая в условиях реальной физической опасности, она позволяет максимально использовать все ресурсы организма, что и обеспечивает выживание в ситуациях, несущих в себе потенциальную угрозу для жизни. Что касается человека, достаточно часто быстрый рефлекторный ответ у него запускается тогда, когда потребности в этом нет. Большинство стрессовых факторов в современном мире не связано с реальной угрозой для жизни. Соответственно в стрессовой реакции, мобилизующей все ресурсы для обеспечения в первую очередь физического ответа, нет необходимости. Более того, она может способствовать развитию серьезных заболеваний и осложнений [3].
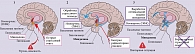
Рефлекторные стрессовые реакции человека не являются адаптивными, поэтому он приобрел возможность контролировать и регулировать свои эмоции и поведение. Осознанный контроль стал возможен за счет активного развития неокортекса и формирования двусторонних связей между эволюционно более древними структурами лимбической системы и префронтальной корой (ПФК) [2, 4]. При первичном столкновении с любой новой стрессовой ситуацией, в условиях неизвестности и невозможности просчитать степень риска миндалина превентивно запускает стрессовый ответ, чтобы быть готовой к быстрым реакциям при возникновении какой-либо угрозы. Поведение человека в этот момент, его эмоциональные реакции скорее рефлекторны и нередко, к сожалению, абсолютно дезадаптивны [1]. В дальнейшем неокортекс анализирует пережитый эпизод: оценивает реальность угрозы, риски его повторения, адекватность поведения и эмоций человека, сопоставляет эту ситуацию с предыдущим опытом [5]. В итоге вырабатывается оптимальная модель поведения, которую человек впоследствии сможет использовать при возникновении похожих эпизодов, что позволяет лучше адаптироваться к ситуации, адекватнее на нее отреагировать и избежать стрессовых реакций. Чем лучше ПФК сможет оценить степень реальной опасности, тем адаптивнее будут эмоциональные реакции, поведение человека и выше его стрессоустойчивость (рис. 1) [1].
Базовые представления об опасности закладываются с детства: по мере ознакомления со страхом у человека формируются функциональные связи между нижележащими структурами лимбической системы и неокортексом (в первую очередь ПФК), которые и обеспечивают дифференцированное восприятие степени угрозы и адекватность последующего ответа [6]. Действительно, методы как структурной, так и функциональной нейровизуализации демонстрируют, что адекватность формирования и развития крючковидного пучка (проводящих путей между лимбическим мозгом и корой) напрямую коррелирует с риском развития аффективных расстройств в поздние годы [7]. По сути ПФК может подавлять рефлекторные реакции, играя роль тормозного контроля [1]. Если механизм не работает, создаются условия для растормаживания миндалины, постоянной генерации стрессового ответа и развития патологической тревоги. Неадекватность когнитивной оценки и управления эмоциями обсуждается как один из основных механизмов развития тревожных расстройств. Неадекватность детского опыта, множество стрессовых факторов, а также нарушение сна (именно ночью происходит обработка и переоценка пережитого эмоционального опыта) рассматриваются в качестве основных причин, способных приводить к развитию подобного сценария [1]. Однако нарушение взаимодействия между корой и миндалиной носит двойственный характер. Несмотря на то что недостаток когнитивной оценки и регуляции обсуждается в качестве приоритетной теории развития патологической тревоги, исследования с использованием функциональной нейровизуализации указывают и на обратную ситуацию: к развитию аффективных нарушений может приводить не ограничение влияний со стороны корковых отделов лобной доли, а, наоборот, их чрезмерная активация [1].
Наряду с анализом и когнитивным подавлением чрезмерного стрессового ответа одной из функций ПФК является прогнозирование опасности [8]. Это позволяет в ряде случаев избежать угрозы либо в условиях неизбежности заранее подготовиться к встрече с ней [8, 9]. Например, у человека, который возвращается домой в темное время суток, запускается фоновый стрессовый ответ: организм заранее приходит в состояние повышенной готовности, расценивая ситуацию как потенциально опасную, поскольку предыдущий опыт подсказывает, что риск возникновения непредвиденных опасных событий ночью выше. Отмечаются все классические признаки симпатикотонии: увеличивается частота сердечных сокращений (ЧСС), повышается артериальное давление (АД), учащается дыхание и т.д. Эта превентивная готовность позволяет активировать ресурсы, быть более внимательным и настороженным и соответственно при необходимости обеспечивает более быструю реакцию.
Как уже отмечалось, в условиях неопределенности, когда когнитивные центры не могут реально оценить степень возможной угрозы, стрессовый ответ срабатывает автоматически, поскольку выживание является базовой приоритетной задачей [8, 9]. К этому предрасполагают и особенности личности, а также детский опыт: люди с исходно «катастрофическим» типом мышления всегда пытаются просчитывать ситуацию и готовиться к худшему. Попадая в условия неопределенности, когда реально спрогнозировать дальнейший сценарий не представляется возможным, они пребывают в состоянии постоянной превентивной готовности, что и закладывает основу развития расстройств тревожного спектра.
Таким образом, гипервозбудимость ПФК с вторичной сенсибилизацией миндалины и постоянной фоновой поддержкой стрессового ответа является вторым потенциальным механизмом развития патологической тревоги [1].
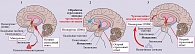
Особый патофизиологический сценарий имеет развитие посттравматического стрессового расстройства (ПТСР), распространенность которого в нашей стране последние несколько лет значительно увеличилась, тенденция к росту сохраняется. Как правило, ПТСР развивается после острой стрессовой ситуации (психологической травмы), связанной с реальной угрозой для жизни человека [10]. При дальнейшей когнитивной оценке подобный опыт расценивается как чрезвычайно опасный, которого всеми возможными способами и средствами необходимо избежать в дальнейшем [1]. В итоге запоминаются все мельчайшие детали пережитого травмирующего эпизода. Это помогает при возникновении риска развития аналогичной ситуации максимально быстро активировать стрессовый ответ и по возможности избежать повторения ситуации (рис. 2).
К сожалению, в дальнейшем это приводит к тому, что любой нюанс или деталь, пусть даже отдаленно связанные с пережитой психологической травмой (запах, звук, какой-то зрительный образ), будут превентивно запускать физическую готовность и рефлекторный ответ, что по сути является третьей ключевой теорией развития тревожных расстройств [10, 11]. В результате человек постоянно пребывает в состоянии стрессовой реакции, его поведение скорее определяется неосознанными рефлекторными действиями и поступками, направленными на выживание, что может приводить к тяжелым, зачастую трагическим последствиям.
Так или иначе, при любом механизме и сценарии развития тревожных расстройств происходит растормаживание миндалины и сцепленного с ней стрессового ответа, что и приводит к развитию когнитивной дисфункции.
Тревога как непосредственный источник когнитивной дисфункции
Даже однократный стрессовый ответ инициирует целый каскад катаболических реакций, обеспечивающих его поддержку: выброс инсулина, приток глюкозы к тканям, увеличение ЧСС и АД для поддержания адекватной перфузии и оксигенации, что делает его крайне энергозатратным [3]. В условиях постоянной активации миндалины и сцепленных с ней центров вегетативной регуляции пациент с тревожными расстройствами находится в состоянии стойкой симпатикотонии, что приводит к доминированию катаболических процессов и постепенному истощению организма [12]. Не случайно длительная стрессовая ситуация, тревога и депрессия неразрывно связаны с таким клиническим синдромом, как астения.
Термин «астения» (греч. centsqsneia, а – лишение, без; esthenos – бодрость, сила) буквально означает «бессилие, отсутствие бодрости». По сути астенический синдром является неким сигнальным механизмом, свидетельствующим об истощении энергетических ресурсов, поэтому может развиваться при чрезмерной нагрузке, после перенесенных тяжелых соматических заболеваний, а также стать закономерным следствием длительного стрессового ответа [13]. Безусловно, наиболее значимо у пациентов с астеническим синдромом будут страдать функции и процессы, которые для своей реализации требуют наибольших энергетических затрат. Для современного человека реализация когнитивной деятельности является наиболее энергозатратной сферой. Соответственно у многих людей астения будет проявляться не столько физической, сколько когнитивной истощаемостью, дефицитом внимания, снижением работоспособности, продуктивности и неспособностью реализовывать привычную когнитивную нагрузку [12].
Таким образом, первой причиной развития когнитивных нарушений у пациентов с тревожными расстройствами считается астенический синдром.
Нарушение восприятия и первичного запоминания информации может быть связано с функциональным выключением гиппокампа – второй ключевой структуры лимбической системы. В условиях стрессовой ситуации и тревоги познавательные процессы переключаются на восприятие исключительно угрожающих стимулов, что затрудняет освоение любой нейтральной и позитивной информации и служит еще одним источником когнитивных проблем [14, 15]. Дело в том, что эволюционно гиппокамп – структура, отвечающая за такие потребности живого существа, как добыча пропитания, размножение, поиск крова. Реализация этих потребностей была возможна только, когда организм считал, что его жизни ничего не угрожает и никакой опасности нет [3]. Достигается это за счет изменения активности так называемого шифта между лимбическими структурами, который регулируется через рецепторы к глюкокортикостероидам (ГКС) [16, 17]. Соответственно в условиях выброса адреналина и кортизола происходит функциональная деактивация гиппокампа в пользу активности миндалевидного тела. С одной стороны, это один из механизмов выживания – организм становится более настороженным к любым угрозам, что позволяет обеспечивать более быстрые рефлекторные реакции, а с другой – приводит к подавлению восприятия любой другой информации, не несущей угрозы, ограничениям нейтрального когнитивного функционирования и нарушению процессов запоминания [18]. Нередко именно жалобы на когнитивную несостоятельность – рассеянность, забывчивость, невозможность сконцентрироваться на новых задачах, что-то запомнить приводят пациентов с тревожным расстройством к врачу. Сама тревога редко фигурирует в качестве ключевого симптома, поскольку в современном мире она считается нормой и элементом критического адекватного восприятия действительности.
Третьей причиной нарушения когнитивных функций у пациентов с тревожными расстройствами является нарушение сна. У 80% пациентов с аффективными нарушениями выявляются значимые расстройства сна, которые могут предшествовать развитию тревоги и депрессии, выступая одним из ключевых факторов риска, а могут развиваться уже по мере появления расстройств тревожно-депрессивного спектра, значительно влияя на качество жизни и определяя высокие риски их хронизации [19]. Представленный выше механизм когнитивной оценки и обработки стрессовых ситуаций и пережитых эмоций реализуется именно во время ночного сна: днем более активно работают системы восприятия, что важно для обеспечения выживания, а ночью, в момент снижения активности, мозг осмысливает пережитый опыт и программирует наиболее оптимальные модели поведения для таких ситуаций [20]. Вполне закономерно, что при недостаточном количестве сна или его качественной неполноценности данный процесс нарушается. Этим обусловлено значимое негативное влияние диссомнических расстройств как на развитие, так и на прогрессирование аффективных нарушений. Кроме того, ночной сон является неотъемлемой частью полноценной когнитивной деятельности. В фазе медленного сна происходит консолидация информации: реактивация краткосрочных воспоминаний и встраивание их на долгосрочное хранение, что служит основой процессов запоминания [18]. Кроме того, как и с эмоциями, мозг анализирует полученную информацию, сопоставляет ее с предыдущим опытом, ищет оптимальные решения, что также является важной частью регуляции поведения человека [21]. В условиях ограничения ночного сна закономерно нарушается процесс запоминания, снижается способность принимать взвешенные адекватные решения, поведение человека становится дезадаптивным и не всегда оптимально для текущей ситуации.
Таким образом, к формированию когнитивной дисфункции у пациентов с тревожными расстройствами обычно приводят астенический синдром, функциональная деактивация гиппокампа при переключении активности в пользу миндалины, а также сопутствующее нарушение сна.
Тревога как фактор риска отсроченных когнитивных проблем
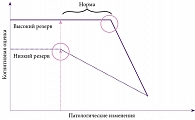
С учетом значимого влияния тревожных расстройств на когнитивные функции можно предположить, что наличие аффективных нарушений ограничивает формирование когнитивного резерва. Когнитивный резерв – эмпирическое понятие, по сути отражающее компенсаторные возможности центральной нервной системы (ЦНС), которые позволяют в условиях хронического или острого повреждения обеспечить функциональную перестройку и адаптацию работы ЦНС с сохранением возможности адекватного когнитивного функционирования (рис. 3) [22]. Показано, что высокий когнитивный резерв – наиболее значимый фактор, снижающий риск развития деменции [23]. У таких людей меньше риск развития когнитивных расстройств после инсульта, черепно-мозговой травмы и других как острых, так и хронических заболеваний ЦНС [24].
Наиболее наглядно значение когнитивного резерва в развитии и течении неврологических заболеваний отразили Y. Stern и соавт. еще в 2009 г. [22, 24]. Так, у двух людей независимо от уровня когнитивного резерва может начаться патологический процесс, приводящий к развитию деменции. По достижении определенного порога изменений в мозге у пациента с низким когнитивным резервом дебютирует когнитивная симптоматика, которая постепенно прогрессирует, через 10–15 лет приводя к полному распаду личности. На этом же этапе у пациента с высоким когнитивным резервом за счет функциональной перестройки и адаптации никаких расстройств, как правило, не выявляется, и он может сохранять относительно адекватный уровень когнитивного функционирования еще достаточно долго. Иными словами, когнитивный резерв не защищает от развития заболевания, но позволяет компенсировать течение патологического процесса, отодвигая сроки клинической манифестации болезни. Социальная изоляция, ограничение контактов, сужение круга интересов значительно влияют на возможности его формирования. Кроме того, с созданием и поддержанием когнитивного резерва неразрывно связан процесс нейрогенеза, особенно в области зубчатой извилины гиппокампа.
Нейрогенез (греч. νεῦρον – волокно, нерв; γένεσις – рождение, возникновение, происхождение) – многоступенчатый процесс образования новых нервных клеток в зрелой ЦНС, являющийся ее адаптивной функцией. За счет формирования новых нейронов у человека формируются новые функциональные связи, коннектомы, которые в дальнейшем и обеспечивают процесс компенсации [25, 26]. Нейрогенез стимулируется активностью рецепторов к серотонину и уровнем трофических факторов, в частности BDNF. В условиях тревоги и депрессии за счет нарушения серотонинергической передачи, а также достоверного снижения уровня BDNF активность нейрогенеза снижается, что приводит к структурным изменениям в области гиппокампа [26, 27]. Современные нейровизуализационные исследования подтверждают уменьшение размера гиппокампа как у пациентов с большим депрессивным расстройством, так и у пациентов с тревогой и нарушением сна [28, 29]. Подавление нейрогенеза служит дополнительным фактором нарушения когнитивного функционирования у пациентов с аффективными расстройствами, а также достоверно увеличивает риск развития деменции за счет снижения компенсаторных возможностей ЦНС. Дополнительно на активность образования новых нейронов способен влиять иммунный ответ: в условиях провоспалительной активации, которая формируется у пациентов с клинически значимыми тревожно-депрессивными расстройствами, процесс нейрогенеза значительно подавляется.
Вероятно, именно нейровоспаление является своеобразным мостиком, соединяющим тревогу и депрессию молодого возраста с повышенным риском последующего развития деменции. Причем негативное влияние воспалительной активации не ограничивается только подавлением нейрогенеза.
Впервые о роли тревоги в генерации иммунного ответа заговорили в 1982 г., когда Г. Хенке и соавт. обнаружили, что стимуляция миндалины (ключевой структуры стрессовой реакции) приводит к развитию язвы желудка, провоцируя системный воспалительный ответ [30]. Исследования последних лет подтвердили, что социальное давление и стресс могут вызывать хроническое воспаление в организме и связаны с более высоким уровнем белков системной воспалительной реакции (интерлейкина (ИЛ) 6 и фактора некроза опухоли альфа), активизацией микроглии и продукцией провоспалительных цитокинов в ее латеральной части, а также повышением пресинаптического высвобождения глутамата [31]. Показано, что использование противовоспалительных цитокинов, например ИЛ-10, может способствовать уменьшению выраженности тревожных расстройств и зависимости от психоактивных веществ. Тем самым иммуномодулирующая терапия была обозначена как потенциальная стратегия для коррекции данных нарушений [32].
Активация симпатической нервной системы при остром стрессовом ответе приводит к выбросу провоспалительных цитокинов, что, по всей вероятности, является частью базового физиологического ответа, подготавливающего организм к риску физического повреждения при столкновении с опасностью. В норме стрессовые провоспалительные эффекты адреналина нивелируются иммуносупрессорными и анаболическими эффектами кортизола [1, 3]. Однако показано, что при тревожных и депрессивных расстройствах происходит снижение чувствительности рецепторов к ГКС, что, с одной стороны, способствует повышению уровня кортизола в крови, а с другой, не позволяет ему реализовывать свою функцию.
Таким образом, у пациентов с тревожными и депрессивными расстройствами отмечается не просто повышение уровня маркеров системного воспаления, а недостаточный противовоспалительный ответ, что подтверждается неэффективностью дексаметазоновой пробы: в ответ на введение ГКС не происходит достаточной выработки противовоспалительных цитокинов. Это косвенно позволяет судить о снижении чувствительности рецепторов к ним [1, 3]. Хронический воспалительный процесс, возникающий вследствие подобных изменений, способствует активации микроглии, инициации окислительного стресса и процессов эксайтотоксичности, что в дальнейшем и приводит к более высокому риску развития нейродегенерации и ассоциированной с ней деменции.
Кроме того, повышенный уровень кортизола, возникающий вследствие низкой чувствительности к нему ГКС-рецепторов, сам по себе ассоциируется с нейротоксическим действием. Так, в рамках клинических исследований показана прямая ассоциация уровня кортизола со степенью нейродегенеративных изменений в лимбической системе [33]. Повышенный уровень кортизола связан с более тяжелой степенью когнитивных расстройств и высоким риском конверсии умеренных когнитивных расстройств до деменции. В исследованиях in vivo и in vitro показано, что кортизол способствует агрегации амилоидного белка, «склеивая» его отдельные компоненты с формированием нерастворимой бляшки [33]. С учетом того что амилоидные бляшки являются одним из основных патогенетических маркеров болезни Альцгеймера, это еще один механизм, который может объяснять более высокий риск развития нейродегенеративной патологии у пациентов с тревожными расстройствами.
Следовательно, тревога может увеличивать риск развития деменции как минимум посредством нескольких механизмов. Она тормозит возможность формирования когнитивного резерва, что ограничивает процессы нейропластичности и адаптации. У пациентов с тревожными расстройствами отмечается постоянная провоспалительная активация за счет развития резистентности рецепторов к ГКС, что приводит к окислительному стрессу, эксайтотоксичности – ключевым патогенетическим механизмам развития как сосудистых, так и нейродегенеративных патологий. Высокие концентрации кортизола вследствие его компенсаторного увеличения за счет изменения чувствительности рецепторов обладают прямым нейротоксическим действием, способствуют агрегации амилоидного белка, что дополнительно усугубляет и без того высокие риски.
Тревога как первый симптом начинающейся деменции
Увеличение риска развития отсроченных когнитивных расстройств при тревоге свойственно пациентам любого возраста. Но если для молодого возраста не все результаты исследований однозначны, то для пожилого прямая связь между тревогой, другими аффективными нарушениями и риском развития деменции не вызывает сомнений [34, 35]. Для обозначения тревоги и депрессии, которые впервые появились у человека в пожилом возрасте, даже существует отдельный термин – аффективные расстройства с поздним дебютом. Тревожно-депрессивные расстройства у лиц старше 60 лет имеют ряд характерных особенностей, что и способствовало выделению их в отдельную группу [34, 35]:
- коморбидны с когнитивными расстройствами и связаны со значительным увеличением риска деменции;
- аффективные нарушения с поздним началом часто атипичны по своим проявлениям и сочетаются друг с другом (апатия с депрессией, депрессия с тревогой и т.д.), а также с психотическими симптомами;
- недостаточно хорошо реагируют на лечение (у 62% не удается получить какой-либо значительной динамики), имеют тенденцию прогрессировать, несмотря на проводимую терапию.
У пациентов пожилого возраста, у которых de novo появлялись аффективные расстройства, в ряде работ отмечалась связь их развития с повышенным уровнем бета-амилоида (маркера нейродегенеративного процесса, в частности болезни Альцгеймера), а также с сосудистыми изменениями. Можно предположить, что тревога и депрессия, дебютирующие у пациентов старше 60 лет, связаны с уже текущим органическим процессом. Прогредиентный характер развития как сосудистых, так и нейродегенеративных заболеваний позволяет объяснить относительную фармакорезистентность аффективных расстройств с поздним дебютом, склонность к прогрессированию, а также частую комбинацию с когнитивными симптомами [35]. Так, за счет анатомической близости расположения гиппокампа и миндалины тревога при болезни Альцгеймера может проявляться одновременно с развитием деменции, а по некоторым данным, даже опережать когнитивную дисфункцию и служить поводом для обращения к врачу. Подобные тенденции справедливы и для депрессии, которая у некоторых пациентов с болезнью Альцгеймера также может оказаться первичным симптомом, что и объясняет выявленную связь аффективных нарушений с амилоидным белком [34]. Кроме того, достаточно часто когнитивные симптомы «закрываются» реакцией на них. Так, пациенты пожилого возраста, даже с самыми ранними проявлениями когнитивных расстройств, начинают беспокоиться о своем будущем, о том, что они могут что-то забыть, вследствие нарушений памяти станут обузой для членов семьи. Это дополнительно провоцирует реактивную тревогу, которая по интенсивности и выраженности может перекрывать когнитивные проблемы. Особенно сильна реакция тогда, когда в семейном анамнезе уже имели место явные расстройства памяти.
В любом случае тревога и депрессия с поздним дебютом должны восприниматься как симптом текущего органического заболевания с очень высоким риском дальнейшего перехода в деменцию. Речь идет не об увеличении риска, а о последовательном развитии различных проявлений неврологической патологии и о том, что тревога в пожилом возрасте может быть первым симптомом начинающихся когнитивных расстройств.
Возможности коррекции тревоги и снижения риска когнитивной дисфункции
Исследование с участием 128 тыс. человек старше 65 лет с тревожным расстройством наглядно продемонстрировало, что даже немедикаментозная коррекция тревоги способствует улучшению когнитивных функций и снижает риск развития деменции (как сосудистой, так и болезни Альцгеймера) [36]. Однако с учетом того, что нередко, особенно в пожилом возрасте, аффективные нарушения развиваются вследствие органических причин, обойтись без медикаментозной терапии, как правило, не представляется возможным.
Поскольку развитие тревоги напрямую связано с нарушением взаимодействия между структурами рефлекторного эмоционального стрессового ответа (миндалина) и структурами, осуществляющими их когнитивный контроль (неокортекс), существуют два ключевых подхода к коррекции тревоги с позиции ее патофизиологических механизмов: попытка усиления контроля со стороны ПФК и подавление гиперактивации структур лимбической системы [1]. Так, мишенью психотерапии, а также антидепрессантов служит скорее усиление регулирующего влияния коры и укрепление контроля над эмоциями, а терапевтический эффект анксиолитиков в первую очередь направлен на снижение избыточного возбуждения миндалины, что приводит к подавлению стрессового ответа и сцепленных с ним соматических и неврологических симптомов [1].
Выбирая антидепрессанты для лечения тревожных расстройств, необходимо учитывать их противотревожный потенциал. Так, большинство селективных ингибиторов обратного захвата серотонина, обладая стимулирующим действием, способны, наоборот, растормаживать тревогу и требовать прикрытия бензодиазепинами или нейролептиками, прием которых нежелателен ввиду частой коморбидности тревоги и когнитивных расстройств [37–39]. Необходимо учитывать влияние на когнитивные функции, особенно у пациентов пожилого возраста, что ограничивает возможности применения трициклических и тетрациклических антидепрессантов с учетом их холинолитического действия. В случае коморбидности тревоги с соматическими и неврологическими заболеваниями неизбежно возникает вопрос об их лекарственном взаимодействии. Хорошим профилем в данном аспекте обладают (эст)циталопрам, сертралин, тразодон, вортиоксетин и венлафаксин, что делает их возможными средствами выбора в лечении тревоги у лиц пожилого возраста. Отличительной особенностью венлафаксина является то, что это препарат с двойным действием, влияющий не только на серотонинергическую, но и на нордаренергическую нейротрансмиссию [40]. Дополнительное усиление норадренергических влияний может способствовать повышению активности, улучшению внимания, что важно с учетом частого пересечения тревожных и когнитивных расстройств. Норадренергические эффекты венлафаксина способствуют уменьшению астении, хронической усталости, что важно как для молодых, так и для пациентов старших возрастных категорий [41]. Кроме того, с учетом частой коморбидности аффективных нарушений и боли препараты с двойным механизмом, действующие на антиноцицептивные системы и способные снижать интенсивность хронической боли, ожидаемо являются средствами выбора. Венлафаксин в капсулах с пролонгированным высвобождением (Велаксин) значительно упрощает прием (один раз в сутки), а при явных когнитивных расстройствах может способствовать лучшей приверженности терапии и большей вероятности соблюдения рекомендаций [42]. Доза варьируется от 75 до 225 мг в зависимости от возраста пациента и выраженности тревоги.
Чаще в лечении тревожных расстройств антидепрессанты комбинируются с анксиолитиками. Классическими анксиолитиками являются препараты группы бензодиазепинов. Будучи агонистами ГАМКергических рецепторов, они тормозят гиперактивность миндалины, обладают наиболее широким потенциалом, обеспечивают быстрый эффект, что особенно важно на старте терапии [1, 43]. Но их применение связано с большим количеством побочных эффектов: привыкание, заторможенность, ухудшение когнитивных функций, провокация слабости и ухудшение астении. Указанные особенности, а также побочные эффекты в отношении сердечно-сосудистой системы, ограничивающие их применение у пожилых людей, делают бензодиазепины не самым лучшим вариантом при сочетании тревожных и когнитивных нарушений или при тревожных расстройствах с высоким риском когнитивной дисфункции. В качестве альтернативы классическим препаратам этой группы можно рекомендовать атипичный бензодиазепин тофизопам. При сохранении всех преимуществ бензодиазепинов тофизопам (Грандаксин) благодаря селективному действию лишь на один из подтипов бензодиазепиновых сайтов связывания лишен побочных эффектов классических представителей группы. Он не вызывает седативного эффекта, не ухудшает когнитивные процессы, не усиливает астенизацию, хорошо переносится и может использоваться пациентами пожилого возраста. Обычно тофизопам применяется не очень длительными курсами в течение двух-трех месяцев в начале терапии и далее по потребности. При необходимости более длительного приема анксиолитиков, что особенно актуально для пациентов с органическими причинами аффективных нарушений, можно отдавать предпочтение небензодиазепиновым анксиолитикам, среди которых наибольшим положительным действием с позиции доказательной медицины обладает буспирон [1, 39].
Таким образом, понимание механизмов развития тревожных расстройств и точек приложения различных противотревожных препаратов позволит оптимизировать подходы к лечению и улучшить качество жизни не только пациента, но и окружающих его людей.
E.E. Vasenina, PhD
Russian Medical Academy of Continuous Professional Education
Contact person: Elena E. Vasenina, hel_vas@mail.ru
Cognitive symptoms are quite typical for various affective disorders and are included in the diagnostic criteria. In recent years, both depression and anxiety are being actively discussed as a significant risk factor determining higher risks of further development of dementia. Thus, the mutual influence of anxiety and cognitive disorders is layered and diverse, however, 3 key variants of their interaction can be distinguished. First, anxiety can be the source and direct cause of cognitive dysfunction. Secondly, anxiety can be a risk factor for the subsequent development of cognitive disorders and dementia. And thirdly, anxiety disorders can be the first symptom of already incipient cognitive decline and dementia. This review will discuss various mechanisms of development of anxiety spectrum disorders, as well as the causes and mechanisms of the close relationship between anxiety and cognitive disorders.
