Лекарственная терапия меланомы кожи 2+ линии
- Аннотация
- Статья
- Ссылки
- English
Введение
Меланома – одна из самых агрессивных опухолей. Метастатическая меланома обладает крайне неблагоприятным прогнозом и, несмотря на малую частоту встречаемости, является причиной смерти более чем 2/3 больных злокачественными новообразованиями кожи.
Количество пациентов с впервые в жизни установленным диагнозом «меланома» в Российской Федерации в 2021 г. составило 4588 человек, заболеваемость – 7,81 на 100 тыс. человек, а среднегодовой темп прироста с 2011 г. – 2,69%. Умерли от данной патологии 3217 человек, средний возраст умерших – 66,2 года (мужчин – 64,5 года, женщин – 66,7 года). Несмотря на огромные достижения последних лет в терапии данной нозологии, в большинстве случаев рано или поздно перед врачом встает вопрос о выборе второй линии терапии.
В данной работе представлен обзор некоторых исследований, которые могут послужить основанием выбора той или иной тактики лечения пациентов с прогрессированием метастатической меланомы.
Критерии выбора терапии
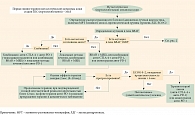
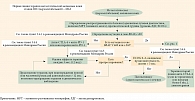
6 декабря 2023 г. на официальном сайте https://cr.minzdrav.gov.ru была размещена актуальная версия рекомендаций Минздрава России по лечению меланомы кожи, что дает возможность практикующим врачам назначать самое современное, только недавно бывшее в рандомизированных клинических исследованиях лечение. В данном документе полно изложены доказавшие свою эффективность варианты терапии. Анамнез (характер течения) заболевания, наличие или отсутствие мутации в гене BRAF, ранее проведенное лечение, степень распространенности метастатического процесса, вовлеченность в него жизненно важных органов, симптомность заболевания, коморбидность пациента и многие другие параметры влияют на принимаемое решение и вероятность достижения успеха планируемого лечения. В рекомендациях Минздрава России представлены последовательность и алгоритмы выбора тактики ведения пациентов (рис. 1 и 2).
На принятие решения о варианте терапии влияют также «Практические рекомендации по лечению злокачественных опухолей» Российского общества клинической онкологии (https://rosoncoweb.ru/standarts/RUSSCO/). Однако окончательный выбор чаще всего остается за конкретным специалистом и консилиумом врачей.
Опираясь на частые сценарии, рассмотрим варианты лекарственной терапии меланомы во 2+ линиях. Наиболее очевидными вариантами выглядят следующие:
- назначить лечение, которое еще не назначали;
- если «всё» уже было назначено ранее, вернуться к опции, которая обладала максимальным эффектом;
- назначить опцию, которая ранее была прекращена по причине токсичности, что дает более обоснованную надежду на достижение эффекта;
- рассмотреть новые, незарегистрированные опции, клинические исследования.
Прогрессирование после применения PD-1-ингибиторов
Терапия анти-PD-1 приводит к длительному контролю над заболеванием примерно у 30% пациентов с метастатической меланомой кожи, однако около 70% пациентов оказываются резистентны к данному лечению.
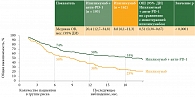
Одно из имеющих наибольшую практическую значимость и нашедшее отражение в рекомендациях Минздрава России исследований было представлено на ASCO 2020 г. В многоцентровое ретроспективное исследование были включены 355 пациентов с меланомой кожи III и IV стадии, прогрессировавших после применения ингибиторов PD-1 в адъювантном режиме или в качестве первой линии терапии. Пациентов стратифицировали на две группы. Первая из них (n = 162) получала антитело к CTLA-4 ипилимумаб в монорежиме, вторая группа (n = 193) – комбинированную терапию ипилимумаб + анти-PD-1. Медиана общей выживаемости (ОВ) составила 20,4 месяца в группе комбинированной терапии и 8,8 месяца в группе ипилимумаба (рис. 3).
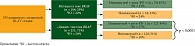
Подгрупповой анализ показал более высокую частоту объективных ответов (ЧОО) при использовании комбинации ипилимумаб + анти-PD-1 по сравнению с монотерапией ипилимумабом в большинстве подгрупп, за исключением пациентов с активирующей мутацией в гене BRAF. ЧОО в данной подгруппе составила 24% среди пациентов, получавших только ипилимумаб, и 21% в группе комбинированного лечения. При «диком» типе BRAF ЧОО составила лишь 10% в группе ипилимумаба и 37% в группе комбинированной терапии (рис. 4).
Примерно у трети (32%) пациентов наблюдались нежелательные явления (НЯ) 3–5-й степени с сопоставимой частотой в обеих группах (31% в группе ипилимумаба, 33% в группе комбинации препаратов). Таким образом, при прогрессировании заболевания на фоне применения анти-PD-1-терапии или после нее на основании полученных данных сочетание ипилимумаба с PD-1-ингибитором показало наибольшую эффективность и является наилучшей опцией для пациентов без активирующей мутации BRAF V600, при наличии же активирующей мутации в гене BRAF ипилимумаб в монорежиме ничем не уступает комбинированной иммунотерапии [1].
Оценка ответа на реиндукцию анти-PD-1 после прекращения моноиммунотерапии в первой линии по любым причинам проводилась в ретроспективном исследовании, опубликованном в 2020 г. В данной работе сравнивалась ЧОО на терапию при реиндукции анти-PD-1 против комбинации ипилимумаб + анти-PD-1. Из 396 пациентов, получивших первую линию анти-PD-1, выделена подгруппа из 78 пациентов, спрогрессировавших после завершения первой линии по любым причинам. Из них 34 пациента повторно получили анти-PD-1, у пяти (14,7%) из которых достигнут объективный ответ (ОО), причем двое достигли полного регресса. В подгруппе из 44 человек, получивших комбинацию ипилимумаб + анти-PD-1, у 11 (25%) пациентов развился ОО, а трое достигли полного регресса [2].
Очередность назначения иммунотерапии и таргетной терапии при метастатической меланоме с BRAF-mut
В исследовании D. Johnson и соавт. изучалась эффективность BRAF/MEK-ингибиторов и анти-PD-1 в зависимости от очередности их применения. Эффективность анти-PD-1- препаратов была выше у пациентов, не получавших ранее таргетную терапию (ТТ) (ЧОО 41% vs 25%). Медиана выживаемости без прогрессирования (ВБП) и ОВ в группе пациентов, получавших ранее ТТ, составила 2,8 и 8,2 месяца соответственно, в то время как в группе получивших в первой линии анти-PD-1 медиана ВБП и ОВ составила 10,6 и 27,6 месяца соответственно.
Аналогичные результаты были получены и при обратном назначении данных линий терапии. Медиана ВБП и ОВ при назначении ТТ пациентам, ранее получавшим анти-PD-1, составила 5 и 10,6 месяца соответственно, тогда как у анти-PD-1-наивных пациентов данные показатели составили 7,6 и 40,3 месяца. В этой работе была выделена подгруппа пациентов, получавших преимущество от обоих видов терапии. Это пациенты, у которых ОО на ТТ сохранялся более 6 месяцев. Они значимо чаще отвечали и на терапию анти-PD-1 (ЧОО 34% vs 15%) [3].
Оптимальная последовательность назначения ТТ и иммунотерапии (ИТ) также изучалась в исследованиях SECOMBIT и DREAMseq. Продемонстрировано, что применение комбинации ипилимумаб + анти-PD-1 с последующей ТТ ассоциировалось со значительным улучшением ОВ по сравнению с обратным порядком (при применении таргетной терапии и последующей комбинации ипилимумаб + анти-PD-1) [4, 5].
Помимо доказанной эффективности назначения ИТ в первой линии по сравнению с ТТ, в работе M. Haist и соавт. был проведен анализ эффективности применения анти-PD-1-препаратов в монорежиме и в комбинации с ипилимумабом. Комбинированная ИТ показала лучшие результаты по сравнению с моноиммунотерапией вне зависимости от последовательности назначения ТТ и ИТ [6].
Прогрессирование на таргетной терапии
В исследовании I.P. da Silva и соавт. изучались эффективность и безопасность применения монотерапии анти-PD-1 и комбинации ипилимумаб + анти-PD-1 после двойной ТТ у пациентов с BRAF-mut-меланомой. Были получены схожие результаты по ВБП и ОВ в обеих группах со статистически недостоверными отличиями (в группе анти-PD-1: ВБП – 3,4 месяца и ОВ – 14,4 месяца; в группе ипилимумаба + анти-PD-1: ВБП – 3,6 месяца и ОВ – 20,5 месяца). Однако в группе ипилимумаба + анти-PD-1 находились пациенты с изначально более неблагоприятными прогностическими характеристиками. Выраженные НЯ ожидаемо развивались чаще в группе, получавшей комбинацию препаратов [7].
Аналогичные результаты по ОВ и ВБП были продемонстрированы в исследовании, проведенном на немецкой популяции. Комбинация ипилимумаб + анти-PD-1 также не имела выигрыша по сравнению с монотерапией PD-1 и ассоциировалась с более высокой токсичностью [8].
Возможности в третьей линии/речеллендж иммунотерапии и таргетной терапии
Во многих работах показано, что независимо от вида опухоли реиндукция ИТ показывает наибольшую эффективность, если ранее ИТ имела определенную эффективность, но была прервана вследствие выраженных иммуноопосредованных нежелательных явлений (иоНЯ) [9–11]. Меланома не является исключением для данной закономерности.
Одна из работ по оценке эффективности реиндукции ингибиторов иммунных контрольных точек при метастатической меланоме проведена в Германии. В анализ включено 570 пациентов, поделенных на четыре группы: первая – речеллендж анти-PD-1 после прогрессировании на анти-PD-1; вторая – речеллендж анти-PD-1 + анти-CTLA-4 после прогрессирования на анти-PD-1; третья – речеллендж анти-CTLA-4 после прогрессирования на анти-CTLA-4; четвертая – речеллендж ИТ после отмены лечения из-за иоНЯ. Наилучшие результаты по достижению ОО и контроля над заболеванием получены в четвертой группе: ЧОО составила 70,2%, частота контроля над заболеванием (ЧКЗ) – 89,5%. Данные показатели в других группах были значимо ниже и примерно соответствовали друг другу [12].
В Memorial Sloan Kettering Cancer Center (Мемориальном онкологическом центре им. Слоуна – Кеттеринга, США) ретроспективно изучали эффективность реиндукции ниволумаба и ипилимумаба у 26 пациентов, завершивших первую линию терапии более чем за шесть месяцев до зафиксированного прогрессирования и повторного назначения. В первой линии ЧОО составила 74%, во второй – 23%. Корреляции между глубиной ответа в первой линии и ответом на терапию во второй линии не зафиксировано. В первой линии ВБП составила 18,5 месяца, ОВ – 35,3 месяца. Во второй линии ВБП равнялась 5,3 месяца, ОВ – 8,4 месяца. Частота иоНЯ в первой линии – 85%, во второй – 58% [13].
Снижение выраженности и риска возникновения иоНЯ при повторном назначении ИТ, прерванной изначально именно из-за токсичности, показано в исследованиях и метаанализах по различным нозологиям [9–11].
При анализе 20 471 248 случаев базы данных VigiBase было выявлено 24 079 (0,1%) случаев иоНЯ, 6123 (25,4%) случая возобновления терапии (из них 452 случая с наличием данных, достаточных для углубленного анализа). После реиндукции ИТ частота развития того же иоНЯ составила 28,8%. Чаще возникали рецидивы иммуноопосредованных гепатитов, пульмонитов и колитов. Кроме того, частота рецидивов была выше при возобновлении терапии анти-CTLA-4 [14].
Согласно рекомендациям Минздрава России по лечению меланомы кожи и слизистых оболочек, возобновление ИТ после развития иоНЯ возможно только после тщательной оценки пользы и риска в случае, если НЯ никогда не достигали 4-й степени по СТСАЕ v 5.0. И возобновление возможно в виде монотерапии анти-PD-1, если в прошлой линии лечения использовалась комбинация анти-PD-1 и анти-CTLA-4 [15].
Если говорить о реиндукции ТТ, прослеживается аналогичная связь между эффективностью таргетных препаратов в первой линии, отменой вследствие НЯ и их повторным назначением.
Проведенный в 2023 г. метаанализ по изучению эффективности и безопасности повторного назначения ТТ включил в себя семь исследований и 400 пациентов. Большинство пациентов на момент начала третьей линии имели метастазы в головной мозг. Получены следующие результаты: контроль над заболеванием достигнут у 65% пациентов, ОО – у 34% пациентов, медиана ВБП составила пять месяцев, медиана ОВ – 9,8 месяца. Метастазы в головной мозг или повышенный уровень лактатдегидрогеназы не показали статистически достоверной взаимосвязи в отношении повышенного риска прогрессирования или смерти. Пациенты хорошо переносили лечение, без ранее не зарегистрированных побочных явлений во время повторного лечения таргетными препаратами [16].
В другом метаанализе от 2018 г. получены более высокие показатели ВБП и ЧКЗ при повторном назначении ТТ и при условии смены ингибитора BRAF. ЧКЗ при назначении той же молекулы составила 29%, а при смене ингибитора – 60%. Аналогичная корреляция прослеживалась и для ВБП – 5,4 месяца при повторном назначении того же препарата и 8,9 месяца при смене молекулы [17].
На ASCO 2023 г. представлены результаты исследования эффективности реиндукции двойной ТТ. Медиана ВБП составила 11,1 месяца, медиана ОВ – 22,2 месяца. При этом полный ответ на первую линию терапии ассоциировался с улучшением выживаемости пациентов при повторном применении BRAFi/MEKi [18].
Роль химиотерапии в лечении метастатической меланомы
Согласно рекомендациям Минздрава России по лечению меланомы кожи и слизистых оболочек, применение химиотерапии должно рассматриваться лишь при невозможности проведения ТТ или ИТ, а также как вариант последней опции лечения у пациентов с прогрессией заболевания после нескольких линий ИТ и ТТ при меланоме с мутацией BRAF [19].
Ретроспективное мультицентровое исследование продемонстрировало низкие показатели ЧОО (12,4%) и ВБП (2,6 месяца) у пациентов, получавших химиотерапию при прогрессировании после ИТ [20].
Среди цитостатиков таксаны показывают наибольшие ЧОО (25%) и ВБП (3,9 месяца), однако при многофакторном анализе различия статистически недостоверны [21].
Заключение
Современные возможности терапии метастатической меланомы позволяют значительно увеличить выживаемость при сохранении качества жизни у пациентов, ранее считавшихся неизлечимыми. Однако рано или поздно этим пациентам необходимо менять или возобновлять системную терапию. Выбор второй и последующих линий осуществляется при старте лечения, поэтому один из подходов, позволяющих проводить системную терапию наиболее рационально, – поиск оптимальной последовательности использования имеющихся противоопухолевых агентов. Так, для пациентов с BRAF-мутацией при отсутствии жизнеугрожающих и симптомных очагов оптимальной опцией для старта терапии является применение ингибиторов PD-1. Для пациентов без мутации в гене BRAF при небольшой опухолевой нагрузке также наиболее рациональная опция – ингибиторы PD-1 в монорежиме. Однако потенциальная польза и риск должны оцениваться мультидисциплинарной командой в каждом конкретном случае. Другой подход, способный изменить цепь событий, запускаемую при старте системной терапии, – поиск новых терапевтических агентов. Так, свою эффективность в клинических исследованиях показывают антитела к рецептору иммунной контрольной точки LAG-3, изучаются препараты на основе опухоль-инфильтрирующих лимфоцитов, противоопухолевые вакцины.
N.V. Zhukova, PhD, V.V. Ovsyanikov, R.V. Orlova, PhD, A.A. Korkina, N.P. Belyak, PhD, S.I. Kutukova, PhD, A.V. Pudina
St. Petersburg State University
Beloostrov High Technology Clinic
City Clinical Oncology Dispensary, St. Petersburg
I.P. Pavlov First Medical University, St. Petersburg
Contact person: Natalia V. Zhukova, drnvz@yandex.ru
Approaches to systemic therapy that have emerged and been implemented in real clinical practice over the past 15 years have significantly changed the perception of metastatic melanoma. Modern targeted and immune therapy often makes it possible to achieve long-term control of the disease, significantly increasing the overall survival rates of patients. However, despite the progress made, sooner or later the question of a second line of therapy arises. The article provides an overview of the main approaches to the selection of the second and subsequent lines of therapy for metastatic melanoma.
